Évolution de la chimie organique depuis 1900

La chimie organique a connu un essor prodigieux depuis plus d’un siècle en raison des progrès de toute nature qui ont permis de mieux la comprendre et d’en tirer parti. Un rapide tour d’horizon de ces évolutions permet de se faire une idée de l’ampleur des changements.
Il existe trois grands problèmes en chimie : structures, mécanismes et synthèse. La structure d’un composé est l’enchaînement de ses atomes constitutifs. Dans les années 1950, l’élucidation de la structure d’un produit contenant 15 atomes de carbone nécessitait quatre ou cinq ans de travail et la destruction de centaines de grammes de ce produit. Actuellement, grâce aux spectroscopies (e.g. spectrométrie de masse et résonance magnétique nucléaire), une telle structure peut être obtenue en un jour avec quelques milligrammes, parfois juste quelques femtogrammes (1fg = 10–15 g) du produit inconnu.
Comprendre la transformation des réactifs
Le mécanisme d’une réaction décrit les changements transformant les réactifs en produits. Seules les structures des réactifs et produits pouvaient être déterminées. Celles des intermédiaires ne pouvaient l’être car leurs durées de vie sont très courtes. Suivant une célèbre boutade, déterminer un mécanisme, c’est retrouver l’intrigue d’une pièce de théâtre en voyant seulement la scène d’exposition et la scène finale. Pendant la première moitié du XXe siècle, utilisant essentiellement la cinétique et l’idée que deux charges de signes opposés s’attirent, l’école anglaise (R. Robinson, prix Nobel 1947, C. K. Ingold) a réussi cet exploit. Ces mécanismes permettaient déjà des prédictions intéressantes, bien qu’un peu simplistes : par exemple, la réaction peut se faire en plusieurs étapes, mais ces mécanismes ne fournissent qu’une vitesse et ne renseignent que sur l’étape la plus lente.
REPÈRES
La chimie a connu un développement explosif. Les Chemical Abstracts ont recensé en 1907, 1950 et 2000 respectivement 7994, 47 496 et 573 469 articles. Il en a résulté des avancées phénoménales. Le présent article est limité à la chimie organique.
Relever le défi des vitesses de réaction
Pour faire une cinétique, il faut mélanger les réactifs, ce qui demande au minimum 10–3 seconde. Pour dépasser cette limite, R. Norrish et G. Porter (prix Nobel 1967) envoient en 10–6 s un premier éclair d’une grande énergie dans le milieu réactionnel, produisant des molécules excitées et des radicaux. Peu après, un éclair de plus faible énergie permet d’analyser le système par spectroscopie. Cette photolyse-éclair est très utile pour la détection et l’identification des espèces fugaces ainsi formées. La méthode développée par M. Eigen (prix Nobel 1967) est basée sur le fait que, dans une réaction réversible, un équilibre s’établit dans lequel les réactions directe et inverse ont des vitesses exactement égales. En perturbant le système (chocs acoustique ou électrique, variations brutales de pression, de température, de densité, etc.) l’une des réactions va réagir plus vite, aboutissant à un nouvel équilibre. Le système étant déjà en fonctionnement, il n’est pas nécessaire de mélanger les réactifs ! L’analyse de la relaxation conduisant au nouvel équilibre permet d’accéder à la constante de vitesse de réaction. Cette méthode s’applique à toutes les réactions réversibles, organiques, inorganiques ou biologiques. La cinétique des réactions se passant en 10–9 – 10–10 s peut ainsi être étudiée.
Réactions sans mécanisme
L’idée que deux charges de signes opposés s’attirent ne s’applique pas toujours. Ainsi, le butadiène n’a pas de charge électrique. Ces molécules n’ont donc aucune raison de s’attirer et de se combiner. Pourtant quand on chauffe le butadiène, il donne facilement un composé à six chaînons :
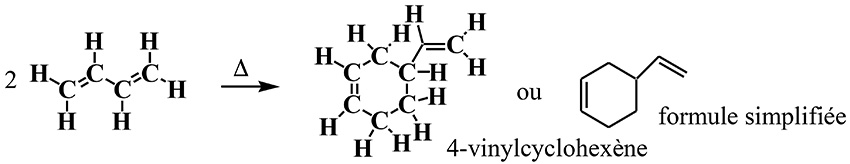
Si on l’irradie, on obtient un composé à quatre chaînons.
Incapables d’expliquer ces résultats, les chimistes ont appelé ces réactions des « réactions sans mécanisme » ! Elles sont cependant importantes car les produits s’obtiennent avec de bons rendements et une stéréochimie bien déterminée. En 1965, R. B. Woodward (prix Nobel 1965 pour ses synthèses) et R. Hoffmann (prix Nobel 1981) ont montré que ces réactions s’expliquent par la conservation de la symétrie des orbitales et en ont déduit des règles de sélection (règles de Woodward-Hoffmann). La méthode des orbitales frontières de K. Fukui (prix Nobel 1981) permet de retrouver ces règles et d’expliquer aussi d’autres résultats, inexplicables par les théories classiques, comme le fait qu’un énolate réagit souvent sur l’atome de carbone alors que l’atome d’oxygène porte une charge négative plus forte.
Calculs quantiques
Les travaux de Woodward, Hoffmann et Fukui prouvent que la chimie est une science quantique. Les calculs quantiques ont donc connu un développement considérable depuis 1970, créant un domaine nouveau, la « chimie computationnelle ». Les travaux combinant étude expérimentale et calculs sont chaque jour plus nombreux.
Ces calculs sont particulièrement utiles pour les espèces fugaces. En fait, un des tout premiers succès de la chimie quantique était de montrer que le carbène CH2 – un carbone divalent – est coudé alors que les expérimentateurs, G. Herzberg (prix Nobel 1971) en tête, pensaient qu’il était linéaire.
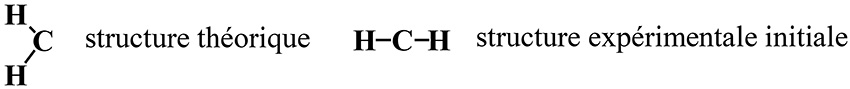
Pour étudier un mécanisme par le calcul, le point de départ est une surface de potentiel donnant l’énergie du système en fonction des positions des atomes. Sur cette surface, les réactifs et produits sont des creux dans les vallées et l’état de transition un col. La différence d’énergie entre le col et les réactifs est l’énergie d’activation. Mais les calculs fournissent aussi les structures des états de transition, inaccessibles à l’expérience, leur durée de vie étant de l’ordre de la picoseconde (1ps = 10–12 s).
Calculs de dynamique
On peut également obtenir une description microscopique des mécanismes (appelée dynamique chimique) en considérant le système comme un point se déplaçant sur la surface de potentiel. Suivant les conditions initiales (répartition de l’énergie entre les composantes, direction des vitesses de départ…), le trajet du point est alors calculé. Il faut calculer de nombreux trajets et les calculs de dynamique sont encore relativement rares. Ils apportent cependant des informations très intéressantes.
Le temps de calcul croissant en gros comme la 4e puissance du nombre d’atomes, les chimistes ne calculent que des modèles, par exemple juste deux molécules de réactifs, sans solvant. Mais la présence de solvant peut changer la réaction.
D’où un grand problème, l’introduction du solvant augmentant sensiblement la taille du système. M. Karplus, M. Levitt et A. Warshel ont reçu le Nobel 2013 pour avoir inventé la méthode QM/MM (Quantum Mechanics/Molecular Mechanics) pour calculer de gros systèmes sans consommer trop de temps d’ordinateur. Elle est basée sur deux remarques : 1) la physique classique est une excellente première approximation ; 2) dans les gros systèmes (enzyme + substrat, protéine + médicament…) le nombre d’atomes intervenant effectivement dans la réaction est petit. Ces auteurs calculent donc la portion « active » par la mécanique quantique et tout le reste par la mécanique newtonienne.
“Une réaction chimique
dure généralement quelques centaines
à quelques milliers
de femto-secondes”
Jets moléculaires croisés et femtochimie
La seconde moitié du XXe siècle voit apparaître également des études expérimentales de dynamique chimique. Deux principales méthodes sont utilisées, les jets moléculaires croisés (D. R. Herschbach, Y. T. Lee et J. C. Polanyi, prix Nobel 1986) et la femtochimie (A. Zewail, prix Nobel 1999).
Dans la première méthode, qui date des années 1960–1970, les réactifs sont envoyés sous forme de jets moléculaires très dilués. Ces jets se croisent dans le vide, la dilution étant telle que les collisions des réactifs se produisent une fois et une seule. La direction et la vitesse de chaque produit sont alors mesurées. Les caractéristiques accessibles comprennent : la répartition de l’énergie entre les translations, vibrations et rotations ; les moments angulaires et leurs orientations dans l’espace ; les variations de rendement avec l’énergie d’impact ; les collisions réactives et non réactives…
Des impulsions lasers de quelques femtosecondes
Les transformations entre réactifs et produits ne pouvaient être étudiées qu’à la fin des années 1980, quand des impulsions lasers de quelques femtosecondes (1fs = 10–15 s) devinrent disponibles. En effet, pour suivre les déplacements atomiques au cours d’une réaction, il faut être capable de détecter des variations de longueurs de l’ordre de 0,1Å, ce qui demande ~10 femtosecondes. Pour suivre les ruptures et formations de liaisons (longueur = 1Å à 2Å en moyenne), il faut donc pouvoir prendre une « photo » du système toutes les 10 fs.
La femtochimie consiste à envoyer sur le système réactionnel une impulsion laser de quelques femtosecondes pour l’activer, puis une deuxième impulsion laser plus faible pour l’analyser. Comme une réaction chimique dure généralement quelques centaines à quelques milliers de femtosecondes, cette technique permet de suivre les déplacements des atomes, donnant pour la première fois les structures expérimentales des états de transition ! La femtochimie permet d’étudier divers problèmes, par exemple celui de la succession (ou la simultanéité) des ruptures de liaisons. Ainsi, bien que CF2I‑CF2I soit symétrique, les ruptures des deux liaisons C‑I ne sont pas synchrones, la première liaison C‑I se coupe au bout de 0,5 picoseconde et la seconde au bout de 50 picosecondes.
La femtochimie a été appliquée à de plus gros systèmes par exemple les « réactions sans mécanisme », les mouvements des molécules d’eau autour d’une protéine…
Assembler des molécules
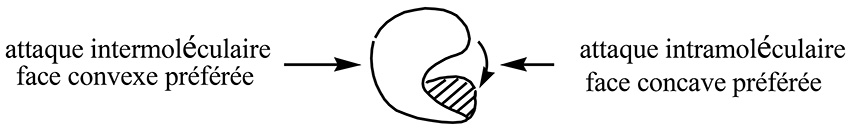
Synthétiser une molécule, c’est assembler ses atomes suivant un arrangement précis. Mais le chimiste ne dispose pas d’atomes libres, seulement des molécules : il y a donc des atomes surnuméraires qu’il faudra éliminer à un moment ou un autre. De plus, quand il fait une réaction entre deux réactifs A et B, il ne peut que mettre ensemble des myriades de molécules de chaque espèce. Ces molécules s’agitent et entrent en collision au hasard : A peut attaquer B par le haut ou par le bas, par la gauche ou par la droite, en avant ou en arrière et chaque attaque pouvant donner naissance à un produit différent. Et pourtant, en mettant à profit la sélectivité des réactions concertées, l’analyse conformationnelle et quelques idées simples (e. g. si la molécule est « courbe », une réaction intermoléculaire est plus facile du côté convexe et une réaction intramoléculaire est plus facile du côté concave), les chimistes ont pu préparer des molécules extrêmement complexes.
Des progrès fantastiques
La synthèse a connu de fantastiques progrès depuis 1950. Nous allons les analyser sous trois catégories : réactifs, méthodes et thèmes directeurs. D’une façon générale, les nouveaux réactifs sont plus doux, tendent à réagir avec une fonction sans toucher aux autres fonctions présentes, pour éviter les étapes de protection-déprotection.
Avant 1950, les organiciens utilisaient une vingtaine d’éléments. Maintenant, la plupart des éléments sont employés pour créer des réactifs. Parmi les éléments des groupes principaux, mentionnons le bore et le soufre qui ont valu à H. C. Brown et G. Wittig le prix Nobel 1979. La réaction d’hydroboration permet de transformer un alcène en pratiquement n’importe quelle autre fonction. La chimie du soufre est très riche, le soufre ayant 9 degrés d’oxydation et les sulfoxydes sont chiraux.
Un domaine en plein développement est la chimie organométallique qui étudie des complexes d’un métal de transition entouré de substituants appelés ligands. Les métaux de transition utilisent les 9 orbitales s, p et d pour faire des liaisons, ce qui permet de les faire dans pratiquement toutes les directions. D’où des structures très variées pour les complexes. Cette chimie est luxuriante car les métaux de transition peuvent recevoir et donner des électrons aux ligands. De plus le nombre d’électrons du complexe peut être modifié en changeant de métal ou son degré d’oxydation. Comme les ligands entourant le métal sont proches dans l’espace, ils peuvent se coupler. C’est une méthode efficace pour créer des liaisons C‑C (important pour la construction des squelettes organiques).
Photochimie, chimie enzymatique, électrochimie…
Des méthodes spéciales permettent de synthétiser des molécules particulières. Ainsi, la photochimie permet de préparer des molécules tendues et la chimie enzymatique des synthèses asymétriques. La liaison CO se coupe difficilement en deux radicaux. C’est pourquoi la chimie radicalaire est utile en chimie des sucres (qui contiennent beaucoup de liaisons CO). Elle est aussi avantageuse pour fonctionnaliser les liaisons CH non activées, un domaine en plein développement. L’électrochimie permet des oxydoréductions difficiles, comme le couplage de deux sites riches en électrons ou de deux carbones en hybridation sp3. La chimie sur support solide (R. B. Merrifield, prix Nobel 1984) est avantageuse pour la préparation des protéines et peptides.
Thèmes directeurs
Nous analyserons un seul thème et mentionnerons brièvement trois autres. Le thème analysé est celui des molécules « impossibles ». En effet, les « lois » chimiques (valence, angles de liaisons, solubilité…) sont approximatives. Pour cerner leurs limites, les expérimentateurs ont synthétisé des molécules contraires à ces lois. Voici quelques exemples pris dans des domaines très différents.
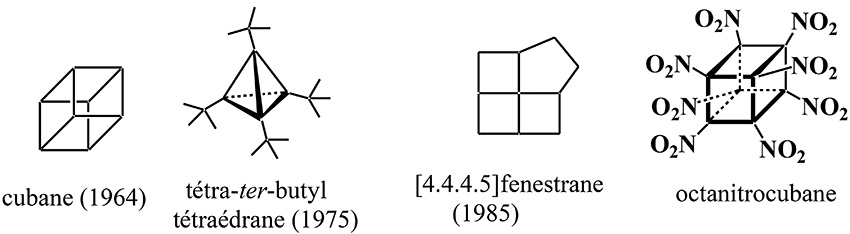
Normalement, le carbone est tétravalent et les liaisons font entre elles des angles de 109° 28’. Les chimistes ont donc préparé des composés avec des angles de 90° (cubane), de 60° (tétra-ter-butyltétraédrane) et un carbone presque plan avec 4 angles de ~130° [4.4.4.5]fenestrane. Ces molécules tendues sont très énergétiques et l’octanitrocubane est l’un des explosifs les plus puissants connus.
Mélanger l’eau et l’huile
L’eau et l’huile ne se mélangent pas. Peut-on fabriquer des substances solubles et dans l’eau et dans l’huile ? Oui, ce sont les détergents formés d’une chaîne hydrophile et d’une tête lipophile. Et des composés insolubles dans l’eau et dans l’huile ? Oui, ce sont les hydrocarbures perfluorés dans lesquels tous les hydrogènes sont remplacés par des fluors. Ils sont utilisés dans les revêtements : peintures antigraffitis, poêles non attachantes, traitements antisalissants… Les perfluorés sont des « Schtroumpfs grognons » qui ne s’aiment pas eux-mêmes. Ils se repoussent, laissant des espaces où peuvent s’insérer des molécules d’oxygène. C’est pourquoi ils peuvent servir de substitut du sang. L’écartement des molécules rend les perfluorés légers. Prenons une molécule de 8 atomes de carbone et branchons-lui une tête hydrophile : on obtient un agent extincteur. Dans des essais en mer par vent de force 7, un feu d’hydrocarbure est maîtrisé en moins de 2 minutes par des solutions aqueuses à 0,1 % de ce produit. L’agent perfluoré flotte sur l’hydrocarbure, entraînant avec lui des molécules d’eau liées à sa tête hydrophile. Cette « eau légère » forme une couche superficielle isolant l’hydrocarbure de l’air. Plus d’oxygène, plus de feu !
Peut-on enfin prendre une entité hydrophile (lipophile) et la faire apparaître comme lipophile (hydrophile) ? Oui, il suffit de lui faire revêtir puis enlever une « tenue de camouflage » comme un éther-couronne. Dans un milieu aqueux, le cation enveloppé par les oxygènes de l’éther-couronne est lipophile grâce aux groupes CH2.
“La chimie fournit
des matériaux à toutes
les autres sciences”
Des innovations prometteuses
Pour terminer, mentionnons trois autres grands problèmes de la chimie.
Le prix Nobel 1987 fut attribué à D. J. Cram, J. M. Lehn et C. J. Pedersen pour la chimie supramoléculaire qui étudie les molécules liées par des interactions non covalentes. Des problèmes de chimie supramoléculaire comme la reconnaissance moléculaire, l’autoassemblage… pourront nous aider à comprendre l’apparition de la vie.
Le prix Nobel 2016 fut attribué à J. P. Sauvage, J. F. Stoddart et B. L. Feringa pour les machines moléculaires. Prenons un homme dont la barbe pousse d’1 mm par jour. Chaque seconde, sa barbe aura poussé de plus d’une centaine d’angströms, ce qui correspond à la taille de ces machines. De telles machines ont de grandes possibilités, notamment en médecine.
La chimie fournit des matériaux à toutes les autres sciences. On sait maintenant fabriquer des polymères plus légers et plus résistants que l’acier, des polymères antimicrobiens, des conducteurs non métalliques (A. J. Heeger, A. G. MacDiarmid, H. Shirakawa, prix Nobel 2000), des céramiques peu fragiles, des verres métalliques, des métaux à mémoire de forme, des gels si légers qui ne courbent même pas une étamine…






