Les biofilms : ces cités de microbes qui font tourner le monde

Longtemps, les bactéries ont été considérées comme des êtres unicellulaires autonomes. Il apparaît maintenant qu’elles forment des communautés complexes enveloppées dans une matrice gélatineuse. Ce sont les biofilms qui peuvent avoir des conséquences néfastes quand ils interfèrent avec des processus d’ingénierie, ou bien lorsqu’ils abritent des pathogènes. C’est pourquoi ils attirent de nombreux efforts de recherche.
Invisibles à l’œil nu, les microbes n’attirent pas notre attention au quotidien, ou bien uniquement lorsqu’un dérèglement du système nous rappelle à quel point nous y sommes vulnérables. Et pourtant, nous baignons dans un monde qui repose sur ces êtres microscopiques.
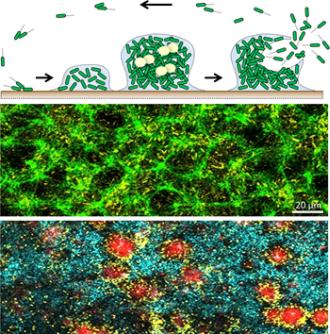
En haut : cycle de développement des biofilms.
Au milieu : interconnexion des cellules bactériennes dans la matrice du biofilm.
En bas : organisation spatiale structurée favorisant la coopération dans un biofilm à 3 espèces (marquées en bleu, rouge ou jaune).
© DR / K. LEE, SCELSE / M. MUKHERJEE, SCELSE
Dotés d’un arsenal prodigieux d’enzymes et protéines aux propriétés diverses, les micro-organismes occupent les niches écologiques les plus extrêmes et sont les acteurs principaux des cycles globaux des éléments essentiels à la vie sur terre (carbone, azote, phosphore, soufre).
Longtemps, les bactéries ont été considérées surtout comme des êtres unicellulaires autonomes, ce qui a permis notamment de grandes avancées dans la compréhension de la régulation génétique et la mise au point de formidables outils moléculaires, à la base des prouesses de la biologie moderne.
Il apparaît maintenant évident que la plupart des bactéries ne vivent pas seules, mais forment des communautés complexes attachées sur les surfaces et enveloppées dans une matrice gélatineuse qu’elles produisent : les biofilms.
A contrario, les bactéries libres en suspension résultent généralement de la dispersion du biofilm et, comme les graines des plantes, servent à étendre la colonisation à de nouvelles surfaces (voir croquis).
REPÈRES
L’organisation sociale du biofilm repose sur la capacité des micro-organismes à communiquer via des signaux moléculaires, à coopérer et partager nourritures et tâches.
De plus, les conditions de couche limite à l’interface solide/liquide et les gradients qui s’établissent dans le biofilm favorisent le développement d’un ensemble hétérogène de cellules différenciées, créant ainsi une communauté aux caractéristiques proches des organismes multicellulaires.
DES BONS ET DES MAUVAIS BIOFILMS
Les interactions entre les membres du biofilm permettent une large gamme d’activités qui peuvent être avantageuses, par exemple pour le traitement des déchets, la réhabilitation des zones polluées, ou encore en médecine lorsque les biofilms de l’hôte défendent contre l’invasion de bactéries pathogènes.
“ La plupart des bactéries ne vivent pas seules, mais forment des communautés complexes ”
En revanche, la quasi-omniprésence des biofilms peut parfois être néfaste quand ils interfèrent avec des processus d’ingénierie, ou bien lorsqu’ils abritent des pathogènes. Ainsi, dans l’industrie, les biofilms peuvent détériorer les membranes de filtration d’eau, souiller les surfaces de transformation agroalimentaire, ou encore augmenter le risque de contamination dans les piscines.
En milieu clinique, les biofilms sont souvent la cause d’infections chroniques pratiquement impossibles à éradiquer. Malgré les avancées technologiques, la redoutable capacité d’adaptation des microorganismes rend souvent le contrôle de ces communautés très incertain.
UNE FORTE RÉSILIENCE ET RÉSISTANCE AUX ANTIBIOTIQUES
Une fois qu’un biofilm est formé, il est très difficile de le déloger, car ce mode de vie offre aux bactéries plusieurs niveaux de protection supplémentaire par rapport aux cellules en suspension :
“ J’ai découvert un signal clé déclenchant la dispersion des biofilms ”
- d’une part, la matrice gélatineuse gène la diffusion de composés antimicrobiens ainsi que l’accès au biofilm des agents du système immunitaire, tout en concentrant les défenses bactériennes telles que les molécules sécrétées capables d’inactiver les antibiotiques ;
- d’autre part, la proximité des cellules favorise la propagation rapide de gènes de résistance ;
- et enfin, d’autres caractéristiques propres comme la présence d’une petite proportion de cellules « persistantes » à métabolisme réduit (presque dormantes), qui tolèrent très bien les traitements antimicrobiens.
Cette résistance accrue peut être un véritable casse-tête. L’utilisation de plus fortes doses est inutile et impossible car cela endommagerait les matériaux ou bien le traitement lui-même risquerait de poser un problème de santé publique.
DÉVELOPPER DE NOUVEAUX OUTILS DE CONTRÔLE DES BIOFILMS
Les biofilms ont attiré de nombreux efforts de recherche et ils commencent à être mieux compris.

Les biofilms ont attiré de nombreux efforts de recherche et ils commencent à être mieux compris. © KKOLOSOV / FOTOLIA.COM
Ainsi, chez certaines espèces, des gènes spécifiques impliqués dans les étapes clés ont pu être identifiés et de nouvelles solutions ciblant l’adhésion, la dispersion, la communication intercellules, ou les messagers intracellulaires ont été mises au point pour améliorer le contrôle des biofilms.
J’ai découvert pendant ma thèse un signal clé déclenchant la dispersion des biofilms : le monoxyde d’azote (NO), une molécule signal universelle dans les systèmes biologiques, qui, quand il est produit dans les biofilms, induit, via le messager secondaire di-GMP cyclique, la dégradation des systèmes d’adhésion et l’activation de la motilité.
Avec des partenaires industriels de l’université où je travaillais à Sydney, nous avons ensuite breveté une série de technologies basées sur la libération de NO. Ainsi, des composés permettant une activation spécifique dans le biofilm peuvent être utilisés pour traiter des maladies infectieuses chroniques.
De plus, nous avons conçu de nouveaux polymères et nanoparticules, capables soit de stocker du NO pour un relargage sur le long terme, soit de catalyser la production de NO à partir de composés présents dans l’eau, et qui peuvent être ainsi utilisés pour des revêtements antibiofilms.
SINGAPOUR À LA POINTE DE LA RECHERCHE
Une fois qu’un biofilm est formé, il est très difficile de le déloger.
© KATERYNA_KON / FOTOLIA.COM
Singapour a récemment investi plusieurs centaines de millions de dollars pour la création du centre singapourien pour l’ingénierie des sciences de la vie environnementale, dont le premier objectif est la compréhension du fonctionnement des biofilms.
En combinant des expertises multidisciplinaires en écologie microbienne, génomique, microbiologie et ingénierie environnementale, ces équipes travaillent à développer et améliorer les bioprocédés guidés par les biofilms.
Ainsi, parmi les projets phares figure la mise au point de nouvelles piles à combustible microbiennes capables de créer de l’énergie à partir d’eaux usées ou l’optimisation de biofilms pour accélérer la transformation de produits chimiques recyclables sans générer de déchets toxiques.