L’impact de la génomique dans la R & D pharmaceutique : une révolution


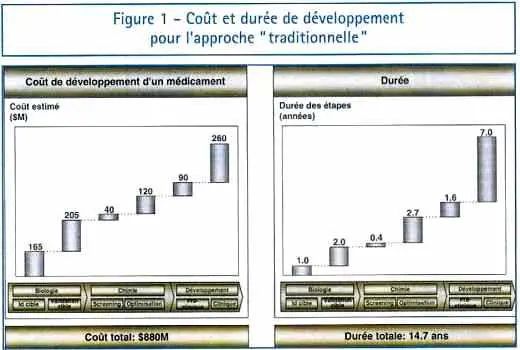
Le processus classique de recherche et développement des médicaments est à la fois complexe, car pluridisciplinaire, et long, car il passe par de nombreuses étapes, de l’identification de cibles biologiques jusqu’aux essais cliniques, strictement réglementés. On estime qu’il faut en moyenne quinze ans et 880 M$ pour développer un médicament en mettant en œuvre l’approche « traditionnelle » des laboratoires pharmaceutiques (voir figure 1).
Le coût total a été estimé en divisant les dépenses de R & D des laboratoires pharmaceutiques par le nombre de médicaments lancés sur le marché. Les trois quarts de ce coût correspondent aux échecs, c’est-à-dire aux molécules abandonnées lorsque des problèmes de toxicité ou d’effets secondaires sont mis en évidence au cours des essais cliniques. En effet, dans l’approche traditionnelle, beaucoup de propriétés de la molécule étudiée ne se révèlent que lors des essais cliniques, soit très en aval dans le processus, à la fois par manque de compréhension des mécanismes d’action et par impossibilité de prévoir les effets dans l’organisme de la molécule. C’est donc principalement l’observation des patients au cours des essais cliniques qui vient valider ou invalider les hypothèses émises par les chercheurs.
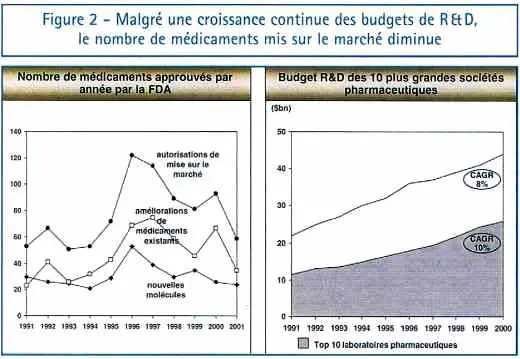
Au cours des dernières années, l’innovation pharmaceutique a ralenti malgré des investissements en R & D toujours plus importants (figure 2). À ceci s’ajoute la part croissante des médicaments à l’efficacité renforcée, plutôt que des produits véritablement innovants, dans les nouvelles autorisations de mise sur le marché. Le déficit d’innovation est amplifié par les choix des laboratoires pour des améliorations progressives qui présentent des risques moindres lors des processus d’essais cliniques, de plus en plus exigeants et coûteux.
Pour maintenir ses niveaux de croissance historique et atteindre les niveaux de croissance recherchés, l’industrie pharmaceutique devra notamment réussir le développement de médicaments innovants répondant plus efficacement aux besoins des malades tout en présentant moins de contraintes d’utilisation et d’effets secondaires. Une amélioration importante de la productivité de la R & D est nécessaire.
L’ensemble des nouvelles technologies et approches apparues ces dernières années dans l’industrie de la biotechnologie constitue la piste principale pour atteindre cet objectif d’innovation. Ces nouvelles technologies permettent d’améliorer la productivité à toutes les étapes du développement d’un nouveau médicament. Cela nécessitera à la fois la contribution efficace des acteurs de la biotechnologie qui prennent le pari risqué de développer ces technologies, et celle des laboratoires pharmaceutiques pour l’application de ces technologies et la commercialisation des produits.
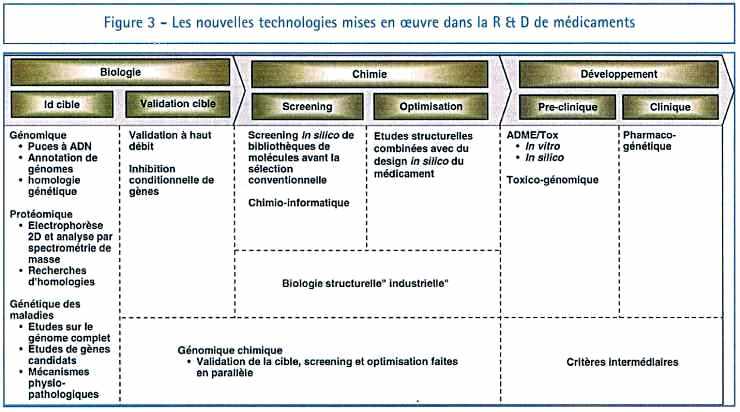
La génomique, rendue possible par le séquençage du génome, est apparue au cours des dernières années. Elle combine l’utilisation des techniques de lecture (séquençage) et d’analyse de variabilité (génotypage) du génome avec des outils puissants de bio-informatique et biostatistique, rendus possibles par la croissance des capacités de calcul. Associée à la protéomique (analyses d’expression des protéines et des interactions protéine-protéine), elle ouvre la voie à une pharmacologie innovante et efficace.
La génomique consiste en l’étude des relations entre les gènes et les maladies (instruction génétique de l’organisme, séquence, régulation et mécanisme). Le but de la génomique est d’utiliser l’analyse de l’ADN pour permettre de comprendre les bases moléculaires des maladies en identifiant les gènes qui leur sont liés. La protéomique permet ensuite une compréhension fine des mécanismes de la maladie au niveau moléculaire.
En comparant des populations de malades et de non-malades, il est possible d’isoler les différences génétiques à l’origine de la maladie. Ces différences peuvent être monofactorielles, lorsqu’une variation sur un gène unique permet d’expliquer le mécanisme de la maladie, mécanisme qui peut être amplifié ou favorisé par des facteurs environnementaux (exemple l’obésité dans le cas du diabète), ou multifactorielles lorsque la maladie (exemple la schizophrénie) résulte de la combinaison de petites variations sur plusieurs gènes, éventuellement renforcée par des facteurs environnementaux.
La génomique révolutionne toute la chaîne de la R & D, et plus directement l’étape de biologie dans le processus d’innovation.
Trois grandes applications existent déjà aujourd’hui :
L’identification de nouvelles cibles pour développer des médicaments. Il s’agit de l’application directe de la combinaison de la génétique et de la protéomique au développement de nouveaux médicaments. Une fois les mécanismes moléculaires compris, il est possible d’utiliser les protéines identifiées comme points de départ pour le développement de nouveaux médicaments. Ces médicaments peuvent prendre la forme de petites molécules, composés chimiques qui viendront moduler l’activité d’une protéine impliquée dans le mécanisme pour en rétablir l’équilibre, ou la forme de protéines thérapeutiques injectables qui viendront contrebalancer directement une déficience dans le mécanisme à l’origine de la maladie.
La qualité des cibles est bien sûr primordiale pour assurer le succès du développement. Au départ, le coût des technologies limitait ces approches à des analyses d’une fraction du génome ; l’évolution des technologies permet aujourd’hui de conduire ces études sur l’ensemble du génome et de déterminer les mécanismes moléculaires les plus importants dans l’origine de la maladie et les plus susceptibles de générer les thérapies les plus efficaces. De nombreux laboratoires pharmaceutiques ont commencé à intégrer ces nouvelles approches dans leur R & D. Ainsi, GlaxoSmithKline a conclu des accords de collaboration avec des sociétés telles que Orchid Biosciences, Sequenom et Illumina pour produire des marqueurs sur l’ensemble du génome.
Le succès de ces approches est lié entre autres à la rigueur de la sélection des individus étudiés et à la qualité des analyses menées ensuite.
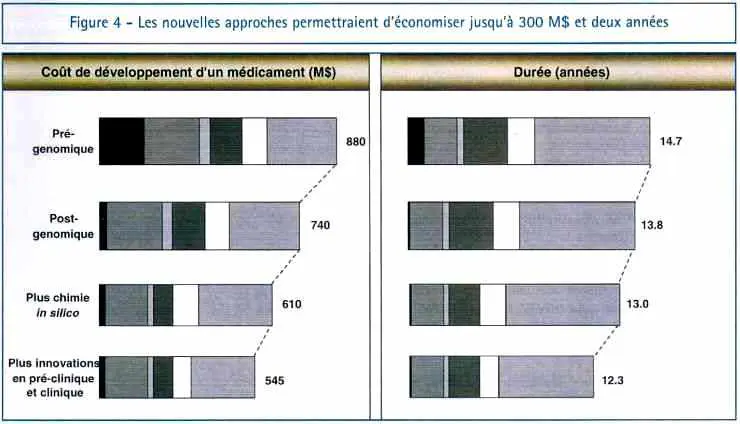
Les investissements considérables nécessaires pour développer un nouveau médicament – 880 M$ et quinze ans en moyenne dans la période prégénomique – pourraient être réduits de plus de 300 M$ et de plusieurs années en appliquant des technologies génomiques. Des gains de productivité seront réalisés à chaque étape de la chaîne de valeur.
Jusqu’à présent, les laboratoires pharmaceutiques ont été pris de court par l’explosion de l’information due à la première vague génomique car il subsistait de nombreux goulots d’étranglement en aval (la chimie et les processus d’essais cliniques). De plus, ces informations résultaient d’études partielles du génome et étaient difficiles à exploiter. La qualité et l’exhaustivité des données augmenteront avec les analyses fondées sur l’étude complète du génome ; elles offriront ainsi de meilleurs points de départ au développement de nouveaux médicaments.
Pour tirer le meilleur parti de ces avancées, les laboratoires devront réaliser des gains d’efficacité aux différentes étapes de la chaîne de valeur pour ne pas ralentir le flux de nouveaux médicaments. S’ils réussissent, un flux continu pourrait être rétabli et les bénéfices attendus pleinement atteints.
Les laboratoires devront aussi faire en permanence des arbitrages entre les investissements nécessaires pour limiter les risques d’échec des composés aujourd’hui en développement et ceux nécessaires à l’acquisition de nouvelles cibles, mieux qualifiées par des analyses plus complètes du génome aux probabilités de succès plus grandes.
Le développement de tests de susceptibilité génétique
Il existe déjà des tests génétiques pour un certain nombre de maladies, comme les cancers du sein et de l’ovaire. Ces tests permettent de définir si le patient présente une mutation génétique d’un ou plusieurs gènes impliqués dans la maladie en question. La crainte que les compagnies d’assurances ou les employeurs n’utilisent les résultats de ces tests au détriment des personnes à risques a poussé les États-Unis à légiférer pour protéger la confidentialité des résultats et éviter les dérives.
Les mécanismes particuliers des patients seront pris en compte pour anticiper leur réaction à tel ou tel médicament, mieux les sélectionner pour les essais cliniques et permettre une meilleure efficacité des prescriptions (pharmaco-génétique). Ainsi, le laboratoire Roche a annoncé en 2003 un test génétique permettant de déterminer comment un patient va réagir à une série de médicaments existants. En effet, on estime qu’environ deux millions de patients américains ont des réactions dues aux effets secondaires des médicaments, qui ont entraîné la mort de 100 000 d’entre eux. Le test, d’après Roche, permettra de déterminer comment le patient métabolise certaines catégories de médicaments. Cela représente une première étape vers le développement de la médecine personnalisée.
Les laboratoires devront relever de nombreux obstacles pour tirer pleinement parti des avancées scientifiques.
Des décisions d’investissement difficiles doivent être prises, en comparant des risques élevés avec des gains potentiels importants. Les sociétés devront décider comment prendre part à la révolution de la génétique, en sélectionnant leurs champs d’investissement propres (technologies et aires thérapeutiques) et le type de collaborations qu’elles devront mettre en place avec les biotechnologies ou les sociétés de diagnostic pour rester cohérentes avec leur politique de tolérance du risque et tenir compte de leurs compétences propres1.
Au-delà du choix des technologies à intégrer et des accords de collaboration, il faut procéder à un rééquilibrage de la chaîne de valeur – en partie en réallouant des ressources, mais surtout en redéfinissant les processus et en gérant la planification et la capacité plus activement. Ainsi, on peut imaginer que les grands laboratoires pharmaceutiques se recentrent sur le développement clinique et la commercialisation des produits, compétences que ne possèdent pas les petites sociétés de biotechnologies.
Il faut établir une infrastructure informatique unifiée – incluant un système centralisé de gestion des connaissances.
Une coordination sans précédent entre le marketing et la R & D sera nécessaire. En particulier, les décisions d’investir sur des maladies et des marchés spécifiques devront être prises en commun par la R & D et le marketing. En effet, la promesse d’une médecine personnalisée a des implications au niveau marketing, tant vis-à-vis des médecins que des patients, dont il faut tenir compte.
Une attention particulière devra être accordée aux aspects éthiques. Les sociétés devront s’assurer de la confidentialité des données génétiques, et se préparer à répondre aux questions ou aux inquiétudes du public.
L’organisation devra s’adapter pour tirer parti de la complexité des offres Biotech, et instituer notamment de nouveaux modes de coopération entre R & D, marketing et business développement
Il faut mettre en œuvre ces divers changements en tenant compte des facteurs humains et comportementaux. L’émergence d’une nouvelle façon de conduire la R & D a en effet des répercussions importantes sur les ressources humaines.
L’émergence de ces nouvelles technologies risque de changer le jeu concurrentiel en profondeur. La capacité des laboratoires pharmaceutiques à relever les défis qu’elles font naître sera déterminante pour leur avenir.
Laurent Billes-Garabedian est vice-président au Boston Consulting Group et responsable du secteur Sciences de la vie du bureau de Paris.
David Picard a passé dix ans au Boston Consulting Group et dirige désormais la société Molecular Acupuncture, spin-off du groupe Serono, qui applique les technologies de génomiques à la compréhension des mécanismes de guérison par acupuncture pour les reproduire sous forme de médicaments.
Leader en France du conseil en stratégie et en organisation, BCG aide les dirigeants et leurs équipes à construire et à mettre en œuvre des stratégies et des modes de fonctionnement susceptibles de conférer à leur entreprise un avantage concurrentiel durable.
1. Les sociétés de Biotechnologies, encore souvent financées par le capital-risque, ont des profils de risque/retour sur investissement différents les rendant mieux à même de prendre les grands paris.



