L’impact des biotechnologies sur la R & D pharmaceutique

L’année 2003 a vu fêter le cinquantenaire de la découverte historique de la structure de l’ADN par James Watson et Francis Crick. Un peu moins d’un demi-siècle après cette invention, le génome humain était intégralement décrypté, ouvrant de nouvelles perspectives dans la connaissance du vivant, tandis que les brevets couvrant les premiers médicaments d’origine biotechnologique commencent à tomber dans le domaine public… Ainsi, d’une découverte fondamentale révolutionnaire est issue, en moins de deux générations humaines, une descendance fertile d’applications, allant de la science la plus pointue à des activités manufacturières banalisées.
Songeons que, sur les trente et une entités moléculaires nouvelles approuvées en 2001 par la FDA (Food & Drug Administration, Agence américaine qui autorise la mise sur le marché des nouveaux médicaments), onze, soit plus du tiers, étaient d’origine biotechnologique. C’est dire que le progrès de la santé publique ne peut plus se passer de ces nouvelles techniques et de leur contribution à l’arsenal thérapeutique et diagnostique. Cette révolution a profondément transformé les processus de la Recherche et Développement (R & D) pharmaceutique.
La R & D pharmaceutique – principes généraux
La R & D est l’essence même de l’industrie pharmaceutique. Si la durée des développements – environ dix ans – et leur coût – aujourd’hui proche du milliard d’euros en moyenne pour une molécule – peuvent la rapprocher d’autres industries de haute technologie telles que l’aéronautique, elle se détache par le caractère quasi totalement autofinancé de cet effort – alimenté par un prélèvement « à la source » proche de 20 % sur le chiffre d’affaires réalisé – et par le degré de risque d’échec.
L’objectif traditionnel : qualité, efficacité, sécurité
Depuis la mise en place des procédures formelles d’autorisation de mise sur le marché, à la suite du drame de la thalidomide, la R & D pharmaceutique a codifié ses processus pour satisfaire les exigences, devenues universelles, des autorités de santé, qui se résument en trois mots : qualité, efficacité, sécurité. Il s’agit pour l’industriel de démontrer que son médicament, parfaitement caractérisé et reproductible dans un contexte manufacturier, possède un rapport bénéfice/risque mesurable et incontestable par rapport à l’abstention thérapeutique.
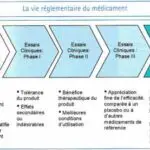
Cette démonstration passe par la réalisation d’un ensemble de tâches étroitement imbriquées (figure 1), organisées dans le moule d’une gestion de projet implacable, qui permettent de définir de manière de plus en plus précise les caractéristiques et les propriétés du produit.
Au plan clinique (c’est-à-dire en ce qui concerne les essais chez l’homme), ce développement passe par l’enchaînement de trois phases : la phase I généralement réalisée sur des volontaires sains1, qui permet de vérifier l’innocuité du produit chez l’homme et de définir la dose maximale tolérée ; la phase II qui permet de déterminer la dose optimale ; la phase III qui permet, sur une population importante, de prouver par des essais contrôlés en double aveugle l’efficacité du produit par rapport à un placebo, et parfois de comparer le produit à ses concurrents existants.
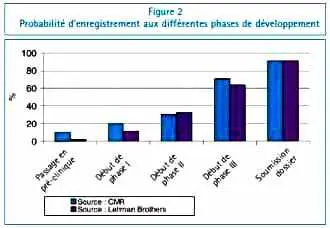
Ce processus de tris successifs conduit à des taux d’attrition importants d’une phase à l’autre, représentés dans la figure 2.
En outre, même la mise sur le marché ne garantit pas un brillant avenir. Chaque année, environ 2 à 3 % des produits enregistrés sont retirés du marché après leur lancement, en dépit de développements impeccables, parce que seule la « vraie vie », l’exposition à la population générale des patients, peut révéler certains effets secondaires très rares mais graves. Sur vingt-cinq ans, 56 produits sur les 548 approuvés par la FDA ont vu leur carrière commerciale brisée par un retrait pur et simple ou par de sévères mises en garde liées à une mauvaise tolérance.
L’objectif implicite : un mode d’action, une efficacité clinique, une utilité dans une population cible
Si la pharmacopée traditionnelle a largement progressé grâce à un processus de tâtonnements et d’observation de la nature – qui a valu à l’humanité les grands progrès de l’ère pasteurienne – la R & D moderne ne saurait s’affranchir d’une démarche mécanistique qui doit, avant tout, identifier un mode d’action reposant sur une compréhension des bases cellulaires ou moléculaires de la maladie et sur un rôle effecteur rationnel de la molécule sur des récepteurs biologiques.
 Parallèlement à la montée des exigences en matière de pharmacologie, l’insolvabilité croissante des systèmes de santé – dans le monde entier – conduit ces derniers, implicitement ou explicitement, à accroître le niveau de démonstration clinique exigé des entreprises pharmaceutiques. C’est ainsi que, dans de nombreux cas, une molécule n’est plus remboursée par les systèmes d’assurance maladie aujourd’hui, si elle ne démontre pas, au-delà de son efficacité intrinsèque, une amélioration du service médical rendu par rapport aux stratégies thérapeutiques existantes – dans le cas contraire, elle sera introduite, au mieux, avec un prix inférieur à celui de ses concurrentes.
Parallèlement à la montée des exigences en matière de pharmacologie, l’insolvabilité croissante des systèmes de santé – dans le monde entier – conduit ces derniers, implicitement ou explicitement, à accroître le niveau de démonstration clinique exigé des entreprises pharmaceutiques. C’est ainsi que, dans de nombreux cas, une molécule n’est plus remboursée par les systèmes d’assurance maladie aujourd’hui, si elle ne démontre pas, au-delà de son efficacité intrinsèque, une amélioration du service médical rendu par rapport aux stratégies thérapeutiques existantes – dans le cas contraire, elle sera introduite, au mieux, avec un prix inférieur à celui de ses concurrentes.
Enfin, les « grandes » pathologies étant à présent relativement bien traitées, la R & D tend à se concentrer, de plus en plus, sur les maladies qui frappent des nombres plus restreints de patients – qu’il s’agisse de pathologies dites « orphelines », ou de sous-populations spécifiques.
L’apport des biotechnologies
Dans ce contexte, quel est l’apport des biotechnologies à la R & D pharmaceutique ? Cet apport s’est matérialisé en deux temps. Dans un premier temps, les biotechnologies ont été, purement et simplement, un mode de production de molécules existant dans le corps humain, ou étroitement dérivées de telles molécules – métier d’ingénieur en quelque sorte, dans une logique manufacturière plus que scientifique. Puis elles ont peu à peu colonisé les laboratoires, révolutionnant les démarches scientifiques et imposant une nouvelle logique dans l’identification de cibles innovantes.
Les biotechnologies de première génération – la fabrication de protéines thérapeutiques
Les biotechnologies traditionnelles sont les héritières de la biologie industrielle, métier dont les pionniers ont été Pasteur au XIXe siècle, et Charles Mérieux, plus près de nous. Deux grandes applications historiques à cette industrie, les vaccins et la transfusion sanguine.
- Les vaccins : cultiver des cellules de germes pathogènes (bactéries ou virus), les inactiver ou les rendre inoffensifs, les purifier, pour en faire in fine un médicament immunogène mais non pathogène.
- La transfusion sanguine : prélever du plasma à des donneurs, le fractionner (selon un procédé d’une logique économique et industrielle proche du raffinage), purifier les composants, pour aboutir in fine à des fractions substituables aux protéines naturelles chez les patients souffrant de déficits congénitaux ou acquis (facteur VIII chez les hémophiles, immunoglobulines2 chez les patients souffrant de déficits immunitaires, etc.). Déjà les bases technologiques des biotechnologies modernes étaient en germe : caractériser, cultiver, purifier. Mais les protéines mises en œuvre étaient extraites à la source et le gène n’était pas manipulé.
| Tableau 1 – Répartition des portefeuilles en fonction de la taille de la population cible | ||
| Taille de la population cible | Produits commercialisés | Produits en développement |
| Petite | 35,7% | 49,8% |
| Moyenne | 30,8% | 30,9% |
| Grande | 24% | 12,7% |
| Très grande | 9,5% | 6,6% |
À partir des années 1980, le développement des techniques permet, d’une part, d’exprimer dans des cellules des protéines exogènes, en intégrant dans leur patrimoine le gène codant pour une protéine d’intérêt, et d’autre part d’immortaliser ces cellules. L’industrie moderne des biotechnologies est née, qui va ainsi développer toute une série de protéines humaines naturelles (ou modifiées à la marge), apprendre à les produire en grandes quantités, et leur trouver des applications.
Parfois ces applications coulent de source, lorsqu’il s’agit de substituer purement et simplement une protéine indispensable à un processus physiologique (ainsi du facteur VIII de recombinaison génétique, qui viendra révolutionner le traitement de l’hémophilie, ou la célèbre érythropoïétine qui stimule la production de globules rouges). Dans d’autres cas, l’industrie devra faire des efforts d’ingéniosité pour trouver une utilité thérapeutique à des protéines telles que les cytokines, certes présentes dans l’espèce humaine, mais dont le rôle est moins bien défini : ce sera le cas notamment dans le domaine naissant de l’immunologie, où les interférons seront développés dans le traitement de l’hépatite B et C (interféron alpha), ou de la sclérose en plaques (interféron bêta).
Quelques belles entreprises naîtront de cette démarche intellectuelle, notamment Amgen, start-up des années 1980, dont la capitalisation boursière atteint aujourd’hui celle de laboratoires pharmaceutiques établis de longue date.
Les biotechnologies d’aujourd’hui – une révolution qui féconde désormais le processus de R & D
Tandis que la liste des protéines humaines utilisables en thérapeutique de substitution tend vers un plateau, le décodage du génome humain et le progrès des techniques de traitement de l’information vont permettre de franchir de nouvelles étapes et d’intégrer l’approche biotech non plus dans les produits finaux, mais dans la démarche intellectuelle du chercheur.
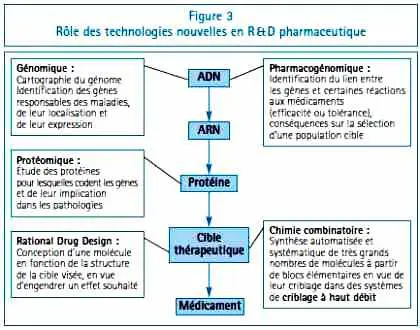 Le décodage du génome humain, graal d’hier, ne résout à vrai dire pas grand-chose en soi. Le livre est certes là, mais tel Champollion découvrant les hiéroglyphes, le chercheur se demande quel est le lien entre la séquence génétique et la réalité biologique. Vont donc se développer de nouvelles sciences (notamment la chimie combinatoire, la protéomique, la pharmacogénomique) visant à éclaircir le lien entre le code, la protéine attachée, et l’activité physiologique dans la vraie vie.
Le décodage du génome humain, graal d’hier, ne résout à vrai dire pas grand-chose en soi. Le livre est certes là, mais tel Champollion découvrant les hiéroglyphes, le chercheur se demande quel est le lien entre la séquence génétique et la réalité biologique. Vont donc se développer de nouvelles sciences (notamment la chimie combinatoire, la protéomique, la pharmacogénomique) visant à éclaircir le lien entre le code, la protéine attachée, et l’activité physiologique dans la vraie vie.
Parallèlement, la maîtrise des techniques d’automation et de robotisation permet d’accélérer de plusieurs ordres de grandeur, et de miniaturiser, les tests pharmacologiques et de rechercher une activité dans des millions d’échantillons dans un temps réduit, là où des mois ou des années de travail auraient été jadis nécessaires. Et la biologie, hier science d’observation, devient une science basée sur la gestion de bases massives d’information. En conséquence, le chercheur du vivant doit assimiler des disciplines échappant à son champ traditionnel – bio-informatique, robotique, électronique, optique – en bref, toutes les sciences de l’ingénieur, et parmi ces dernières une capacité toute particulière, celle d’agir comme un intégrateur, comme un systémicien.
L’objectif, en termes de processus de gestion de la R & D, est ici de multiplier de plusieurs ordres de grandeur le nombre de cibles moléculaires potentielles en accédant à des bibliothèques de gènes, de les cribler de manière impitoyable grâce aux moyens nouveaux fournis par les modèles moléculaires, cellulaires ou animaux issus du génie génétique, et de ne sélectionner que les séquences disposant théoriquement de la plus grande probabilité de réussite. Par rapport aux probabilités de passage d’une phase à l’autre évoquées ci-dessus, on verrait ainsi un taux d’attrition significativement plus élevé en amont (compensé par une créativité décuplée de la synthèse chimique ou biologique), et l’on parviendrait en revanche à rendre beaucoup plus probables les transitions des phases ultimes – étapes les plus coûteuses du développement.
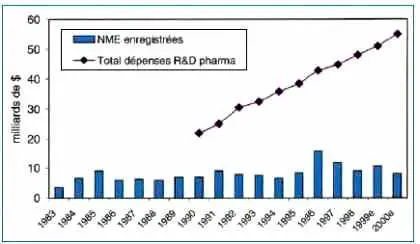
Cette promesse, omniprésente dans toutes les grandes conférences pharmaceutiques depuis la fin des années quatre-vingt-dix, tarde à vrai dire à se concrétiser dans ses résultats, et l’industrie pharmaceutique passe actuellement, paradoxalement, par une phase d’étiage en termes d’enregistrements.
En effet, le basculement des méthodes de recherche et de développement vers la vision messianique du « tout génétique » ne peut porter ses effets qu’au terme d’une génération de développement de nouvelles molécules, soit une bonne dizaine d’années. Les tout premiers produits « ciblés » commencent aujourd’hui tout juste à atteindre le marché. Et c’est là que les acteurs concernés vont découvrir de nouveaux obstacles – non plus scientifiques mais organisationnels.
Les défis de demain – adapter les systèmes de santé pour la distribution d’une médecine personnalisée
On voit bien que le processus visant à identifier les maladies par leurs causes génétiques devrait permettre, de manière ultime, d’adapter les traitements aux patients. Grâce aux nouvelles technologies se dessine l’espoir d’une médecine personnalisée, qui permettrait d’identifier précisément les causes, souvent multifactorielles, du syndrome pathologique dont souffre M. Dupont et de les distinguer de celles qui affectent M. Durand, pourtant atteint cliniquement d’une symptomatologie très voisine. Ainsi, le concept « consommation de masse » du médicament d’aujourd’hui (une molécule unique pour traiter tous les patients), qui a vu le succès des médicaments dits « blockbusters« 3, céderait le pas à une prise en charge individuelle qui pourrait s’appuyer sur des techniques de diagnostic.
 Sont ainsi apparus sur le marché, d’ores et déjà, des traitements du cancer du sein dont l’efficacité ne peut être attendue que chez les femmes porteuses d’un certain gène. La thérapeutique de demain pourrait généraliser ce concept et identifierait chez chaque patient, de manière prédictive, son caractère de « répondeur » ou de « non-répondeur » à un certain type de traitement, ainsi que son aptitude à bien tolérer le médicament.
Sont ainsi apparus sur le marché, d’ores et déjà, des traitements du cancer du sein dont l’efficacité ne peut être attendue que chez les femmes porteuses d’un certain gène. La thérapeutique de demain pourrait généraliser ce concept et identifierait chez chaque patient, de manière prédictive, son caractère de « répondeur » ou de « non-répondeur » à un certain type de traitement, ainsi que son aptitude à bien tolérer le médicament.
Ne nous méprenons pas cependant. Cette vision idyllique et rationaliste ne trouvera sa voie qu’au prix de profondes modifications des systèmes de santé dans le monde entier. Car ces derniers sont aujourd’hui organisés pour bien administrer des traitements de masse. Du médecin à l’industrie pharmaceutique en passant par l’hôpital, tous les acteurs ont été formatés pour un monde standardisé, fondé sur la productivité et l’effet d’échelle.
C’est dire qu’il importe pour l’industrie biopharmaceutique, si elle croit en son nouveau paradigme de recherche, de se pencher rapidement sur l’organisation des systèmes de santé, et d’y jouer un rôle actif d’aiguillon, en suscitant une réflexion sur les conditions du recours aux nouvelles stratégies thérapeutiques issues de la génomique. Ce n’est que par une profonde mutation de la production de soin, tournée – à nouveau, devrait-on dire – sur la prise en compte de l’individu, que les innovations scientifiques de demain pourront se transformer en succès commerciaux.
___________________________________________
1. À l’exception du cancer où les phases I se font généralement chez des malades.
2. Anticorps.
3. Médicaments réalisant un chiffre d’affaires mondial de plus d’un milliard de dollars.