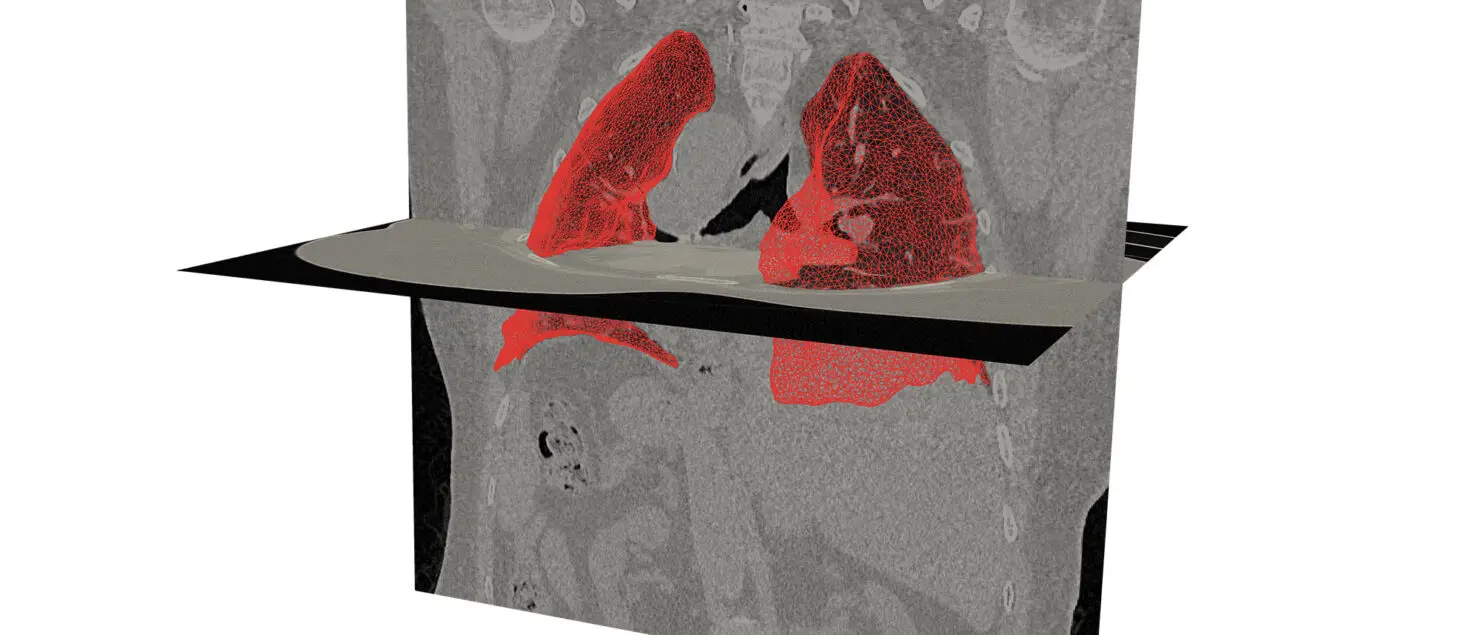
Mécanique pulmonaire personnalisée : modélisation, estimation et application à la fibrose pulmonaire

Au cours de sa thèse effectuée dans l’équipe MΞDISIM, jointe entre l’Inria et le Laboratoire de mécanique des solides de l’École polytechnique et soutenue en décembre 2020, Cécile Patte (D20) a développé un jumeau numérique du poumon, personnalisé à chaque individu, en vue de diagnostiquer et traiter la fibrose pulmonaire idiopathique. Ses travaux de recherche en biomécanique lui ont valu le prix Jeunes Talents France 2020 de la fondation L’Oréal et de l’Unesco.
La médecine in silico, aussi appelée médecine numérique, est l’utilisation d’outils numériques en médecine pour aider le diagnostic et le pronostic de maladies, les procédures chirurgicales, les traitements ou encore les essais cliniques. Déjà largement utilisées dans les domaines de l’aéronautique et de l’automobile, les approches numériques ouvrent de nouvelles perspectives dans le domaine des soins de santé, ce qui fait de la médecine in silico un domaine émergent et prometteur. L’évolution rapide de la discipline est motivée par des questions de société comme le désir de meilleurs soins et est permise par le développement de nouveaux modèles mathématiques, combiné à une augmentation de la capacité de calcul. Ces derniers aspects techniques ont connu un fort essor au cours des dernières décennies et sont maintenant en mesure de répondre aux besoins de la médecine in silico.
Les jumeaux numériques
Bien que les approches statistiques soient largement utilisées, le travail présenté ici se concentre sur une autre sorte d’outils numériques, les modèles physiques. Il s’agit d’équations mathématiques qui décrivent des phénomènes physiques, tels que les fonctions biologiques d’organes ou même du corps entier. Le modèle numérique d’un organe reproduit son fonctionnement réel dans un environnement virtuel et devient dès lors le jumeau numérique de l’organe réel. Il peut être mis à jour en temps réel avec des données provenant de l’organe réel afin de rester une copie conforme dans le temps. Un tel jumeau numérique est très utile car il permet de réaliser des tests, d’étudier des hypothèses, d’évaluer l’impact de la modification de paramètres, etc., sans toucher à l’organe réel. Ces modèles, quand ils sont spécifiques à un patient, apportent des informations sur l’état du patient qu’il n’aurait pas été possible de mesurer et peuvent prédire l’évolution de son comportement futur. Ils sont donc une aide précieuse pour les décisions cliniques et offrent de nouvelles possibilités à la médecine.
« Le jumeau numérique d’un organe reproduit son comportement réel dans un environnement virtuel. »
L’exemple de l’application au domaine cardiaque
La médecine in silico peut être appliquée à une grande variété de domaines et le système cardiaque est sans doute celui dans lequel les modèles sont les plus avancés. Par exemple, le modèle cardiaque développé dans l’équipe MΞDISIM (Mathematical and Mechanical Modeling with Data Interaction in Simulations for Medicine) calcule, à partir de données mesurées chez un patient, des quantités d’intérêt impossibles à mesurer, comme la contractilité du myocarde, ce qui permet d’évaluer la présence et la localisation de pathologies cardiaques. Il peut aussi aider les chirurgiens, dans le cadre d’une thérapie de resynchronisation cardiaque, à localiser la meilleure position pour la stimulation et prédire sa réussite ou son échec, et ainsi éviter une intervention risquée à un patient à forte probabilité d’échec. Enfin, il rend possible la surveillance cardiovasculaire de patients en soins intensifs en apportant de nouveaux indicateurs sur l’état physiologique des patients, utiles pour guider les choix thérapeutiques. Ce sont ces exemples incroyables qui m’ont donné l’envie de rejoindre l’équipe MΞDISIM pour y réaliser une thèse. Pour ma part, j’ai travaillé à développer un modèle numérique, non pas du cœur, mais du poumon.
L’application de la fibrose pulmonaire en ligne de mire pour ma thèse
La modélisation des poumons peut en effet répondre à des enjeux cliniques de maladies pulmonaires, qui comptent parmi les causes principales de mortalité dans le monde. Parmi elles, les maladies interstitielles pulmonaires entraînent une dégradation du tissu pulmonaire et notamment de sa structure alvéolaire, porteuse de la fonction vitale de l’organe. La forme la plus fréquente est la fibrose pulmonaire idiopathique (FPI), maladie chronique progressive au pronostic très sévère, qui se caractérise par une accumulation de tissus fibreux et qui entraîne l’épaississement, la rigidification et la destruction des parois alvéolaires. Ces caractéristiques impliquent une baisse de l’efficacité des échanges gazeux et une perte d’élasticité de l’organe. Les patients souffrent alors de difficultés respiratoires s’aggravant avec le temps.
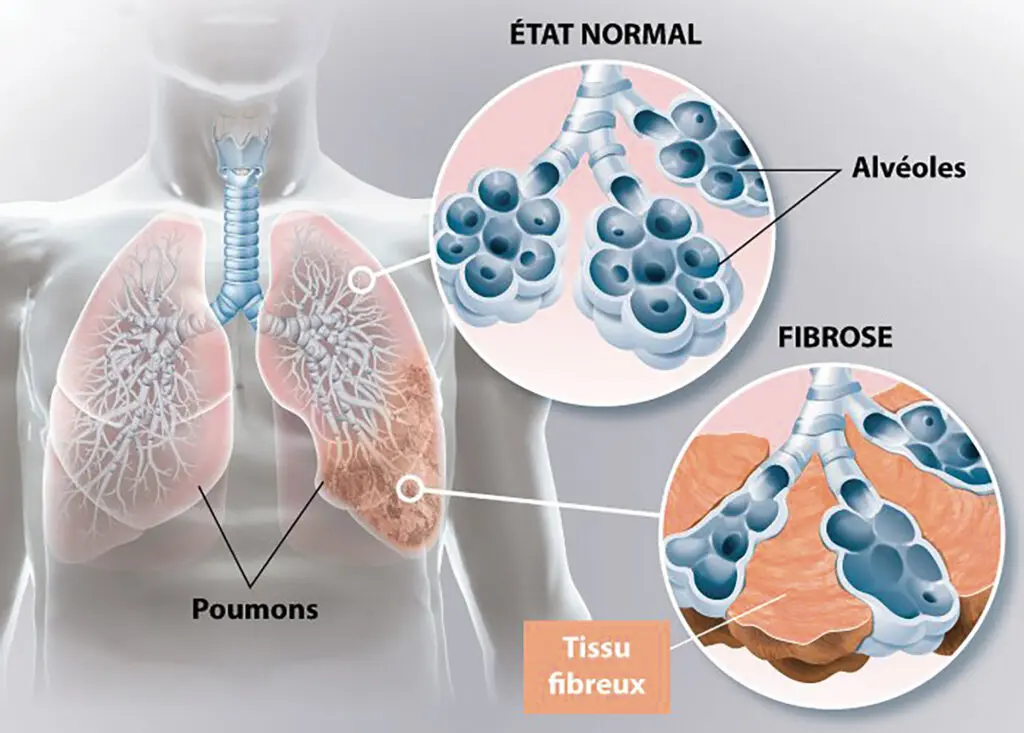
Une maladie encore mal comprise
Cette maladie reste actuellement mal comprise, mal diagnostiquée et mal traitée. En effet, même si positivement corrélée à des facteurs tels que l’hérédité ou le tabagisme, la cause directe de la maladie est largement inconnue (d’où le qualificatif « idiopathique »). De même, la voie de progression reste mal comprise, même si le rôle régulateur de la mécanique semble prépondérant. Une hypothèse a été émise d’un cercle vicieux mécanique ayant lieu chez les patients, au cours duquel la fibrose entraînerait de plus grandes contraintes mécaniques dans le tissu pulmonaire, qui induiraient à leur tour plus de fibrose. Enfin, la maladie reste difficile à diagnostiquer, et mal soignée puisque les médicaments existants ne font que ralentir la progression mais ne la guérissent pas. Les problématiques cliniques autour de cette maladie sont donc nombreuses et l’idée de ma thèse est d’y répondre par le développement d’un modèle numérique de poumon. Le but est de mieux comprendre l’impact de la maladie sur la mécanique pulmonaire, ses mécanismes d’évolution, mais aussi d’améliorer son diagnostic et son pronostic chez les patients. J’ai eu la chance de pouvoir collaborer tout au long de ma thèse avec des médecins de l’hôpital APHP Avicenne, à Bobigny, qui sont confrontés à cette maladie.
Mon travail de thèse s’est organisé autour de deux axes : le développement théorique d’un modèle de poumon générique ; puis la personnalisation du modèle à chaque individu à partir de l’utilisation de ses données cliniques.
Le poumon, un organe complexe à modéliser
Comment procède-t-on pour modéliser le poumon, un organe profondément complexe ? Nous avons chacun deux poumons, d’environ 20 cm de hauteur, situés dans notre cage thoracique, qui se gonflent et se dégonflent quand nous respirons. En les examinant de plus près, on découvre qu’ils sont composés chacun de plusieurs lobes, eux-mêmes divisés en plusieurs lobules. Ces sous-divisions se poursuivent jusqu’aux plus petites unités pulmonaires que sont les alvéoles, de 300 µm de diamètre, dans lesquelles se réalise la fonction principale des poumons : le passage de l’oxygène dans notre sang pour alimenter nos organes, d’une part, et le rejet du dioxyde de carbone de notre sang vers l’atmosphère d’autre part. On peut donc étudier le poumon à différentes échelles selon le phénomène étudié : la déformation des poumons à l’échelle de l’organe (ou échelle macroscopique) ou la diffusion gazeuse à l’échelle alvéolaire (ou échelle microscopique). Une autre complexité de cet organe réside dans sa composition. Le poumon est à la fois composé de tissu biologique, qui lui donne sa structure, mais aussi d’air, qui emplit les voies aériennes et les alvéoles, et de sang, présent dans le système vasculaire pulmonaire. Enfin, la variété des phénomènes physiques ayant lieu dans cet organe constitue une troisième complexité. Les poumons peuvent être étudiés selon le point de vue de la circulation de l’air dans les voies aériennes, selon le point de vue des interactions chimiques et biologiques qui ont lieu entre les composants, ou encore selon le point de vue de la déformation des tissus. Les poumons sont donc des organes multiéchelles, multiphasiques et multiphysiques. Un modèle de poumon peut difficilement représenter l’ensemble de ces complexités et oblige à faire des choix, ceux-ci étant guidés par la finalité visée pour le modèle.
« Les modèles de poumon sont personnalisés en s’appuyant sur les données d’imagerie médicale des patients obtenues en routine clinique. »
Le développement théorique d’un modèle numérique de poumon
Dans le cadre de ma thèse, le modèle de poumon que j’ai développé cherche à répondre aux problématiques de la FPI à l’échelle macroscopique. Ainsi, la physique choisie pour décrire le poumon est la mécanique des solides. Le matériau considéré est un paramètre clé, car il diffère entre une personne saine et un patient atteint de FPI. En effet, la FPI impacte la compliance des poumons, c’est-à-dire leur élasticité ou leur capacité à se déformer. De plus, il a été choisi de prendre en compte l’aspect multiphasique, c’est-à-dire de considérer le poumon comme une éponge emplie d’air, afin de pouvoir traduire le changement de structure lié à la maladie. Ce champ de la physique qui regroupe ces caractéristiques est la poromécanique. En plus de l’utilisation des équations de la poromécanique, développer un modèle de poumon qui reproduit son comportement au cours de la respiration nécessite de bien comprendre la physiologie pulmonaire, afin de reproduire les efforts que subit le poumon par son environnement (la cage thoracique et le diaphragme notamment), ainsi que de bien prendre en compte les propriétés des matériaux qui sont spécifiques au tissu pulmonaire. En effet, une particularité d’un modèle poromécanique est de considérer la porosité du poumon.
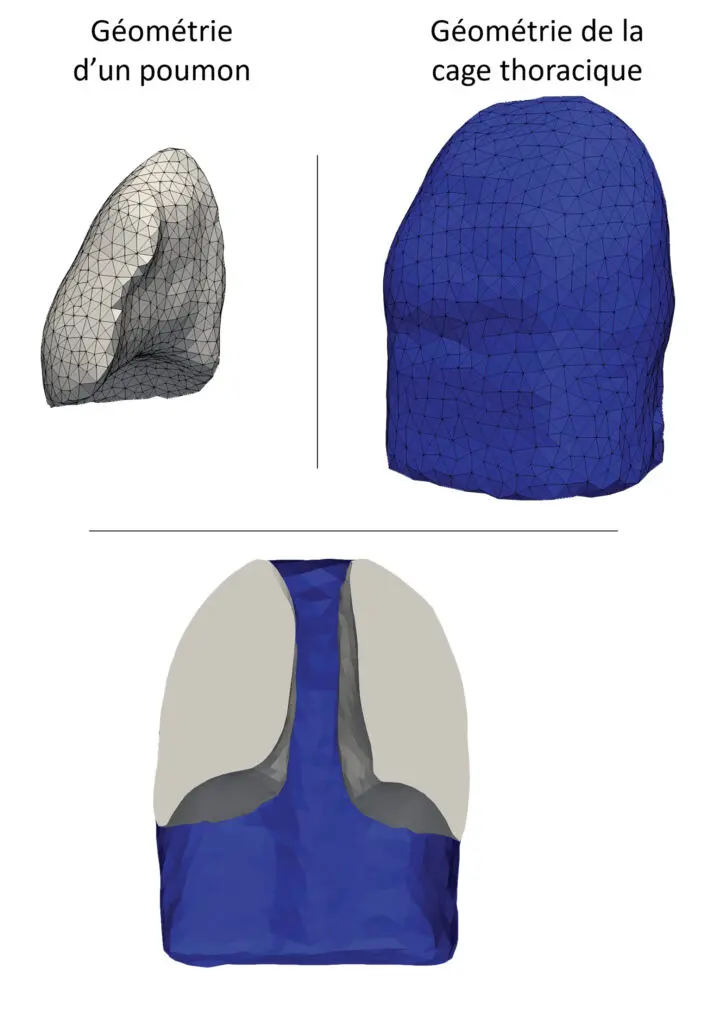
Des données…
À ce stade, le modèle reste très général. Pour le rendre spécifique à un patient et ainsi créer la copie virtuelle de ses poumons, les données du patient sont essentielles. Une fois recueillies, elles sont incorporées dans le modèle. Pour ne pas alourdir le parcours clinique du patient, il est important de considérer des données qui sont déjà obtenues en routine clinique. Chez les patients souffrant de FPI, l’examen principal est un examen d’imagerie médicale par scanner, qui permet de réaliser deux images en trois dimensions de leur thorax, une en début d’inspiration, l’autre en fin d’inspiration. En vue du modèle, des informations sur les pressions pulmonaires pourraient aussi être utilisées. Cependant, elles imposent des techniques invasives et ne sont pas obtenues en routine clinique sur les patients atteints de FPI.
… pour construire un modèle personnalisé à chaque individu
Nous avons maintenant tous les éléments nécessaires pour construire le poumon numérique d’un patient : un modèle de poumon et des données cliniques du patient. Il ne reste qu’à les faire interagir. Comment procède-t-on ? De nombreux éléments de modèle se personnalisent à partir des images de manière directe avec des techniques de traitement d’images : la géométrie de l’organe, propre à chaque individu ; sa porosité, liée aux nuances de gris des images ; et le déplacement de la cage thoracique, en comparant par corrélation d’images les deux images obtenues de l’inspiration et l’expiration. Un élément, cependant, est obtenu de manière moins aisée. Il s’agit des propriétés du matériau, qui sont spécifiques à chacun et ne peuvent pas être mesurées (à moins d’extraire un morceau de poumon du patient afin de réaliser des essais mécaniques, ce qui n’est bien sûr pas faisable sans un acte invasif et potentiellement dangereux). Une stratégie est donc mise en place pour les estimer en utilisant des techniques d’optimisation mathématique. Le problème consiste à minimiser l’écart entre le modèle et les données. Pour cela, on compare le déplacement du poumon calculé par le modèle pour des propriétés matériaux données avec le déplacement du poumon calculé entre les deux images du patient. On regarde l’écart entre les deux ; puis l’opération est répétée avec d’autres propriétés matériaux, jusqu’à réduire cet écart. Une fois que l’écart cible est atteint, on a alors estimé les propriétés matériaux du patient puisque le modèle de poumon se comporte comme dans les données d’observation. Le modèle numérique est alors une copie du poumon du patient.
L’épreuve de l’application
Lors de ma thèse, j’ai personnalisé le modèle à trois patients atteints de FPI. Chez chacun d’entre eux, deux régions ont été repérées, une région saine et une région malade, chacune avec des propriétés matériaux distinctes. La personnalisation du modèle de poumon à ces trois patients a permis d’estimer les propriétés matériaux de chacune de ces régions séparément. À l’exception de l’un des patients chez qui les données ont été difficiles à exploiter, les autres ont présenté une région malade moins compliante que la région saine. Ces résultats sont cohérents avec le fait que la maladie tend à rigidifier les poumons. De plus, le ratio entre les compliances de chacune des deux régions est calculé et pourrait devenir dans le futur un nouveau biomarqueur, fondé sur la mécanique, utile aux médecins pour diagnostiquer la maladie. L’obtention de cette grandeur, régionale, est une avancée majeure car elle ne pouvait pas être obtenue auparavant par les moyens traditionnels, qui caractérisent des grandeurs globales. C’est le développement d’un modèle numérique qui donne accès à cette grandeur régionale. L’hypothèse d’un cercle vicieux mécanique a aussi commencé à être étudiée. En effet, chez les patients étudiés dans la thèse, il a été observé que des zones avec des contraintes mécaniques plus élevées étaient présentes à l’interface entre les régions saines et les régions malades. Cette observation va dans le sens de l’hypothèse, puisque ces surcontraintes activeraient les cellules pour fabriquer plus de fibres, ce qui contribuerait ainsi à la propagation de la maladie.
Une première pierre pour de multiples applications
Finalement, mon travail de thèse est une première brique au développement d’un jumeau numérique de poumon. Il a apporté une preuve de concept sur l’apport d’un modèle poromécanique de poumon pour diagnostiquer la FPI. Une validation sur une cohorte plus large de patients est encore nécessaire. De plus, un long travail est à faire pour que le modèle soit utilisé en routine clinique : alors qu’actuellement certaines étapes sont manuelles et fastidieuses, il faudra développer un logiciel, utilisable facilement par les médecins, qui traitera automatiquement toute la chaîne, depuis les données du patient jusqu’à la création du jumeau numérique de poumon. À plus long terme, ce modèle ouvre de nombreuses perspectives. Il permettra d’améliorer la compréhension de la maladie en étudiant l’hypothèse d’un cercle vicieux mécanique. De plus, une composante multiéchelle pourra être ajoutée au modèle pour mieux comprendre la manifestation de la maladie à l’échelle microscopique. Appliqué à différents moments de la maladie du patient, le modèle permettra aussi de suivre l’évolution de la maladie et pourra à terme la prédire, afin que les médecins puissent adapter la stratégie médicale. On peut aussi imaginer que le modèle puisse être utilisé lors du développement de médicaments, en étudiant leur impact sur la mécanique pulmonaire et donc sur la santé du patient. Finalement, on peut aussi envisager que d’autres pathologies pourraient en bénéficier, comme la Covid-19 ou encore les maladies induites par les ventilateurs pour les patients en soins intensifs. Un grand nombre de ces perspectives est traité actuellement par deux doctorants et un postdoc qui poursuivent ce travail dans l’équipe MΞDISIM.
Cécile Patte (D20)
À l’issu de sa thèse, Cécile Patte a rejoint le groupe Air Liquide en tant qu’ingénieure R & D en modélisation mécanique. Elle travaille au développement de modèles mécaniques afin d’aider au dimensionnement d’équipements industriels et de prédire leur durée de vie.
Informations sur la thèse
Cécile Patte a effectué sa thèse entre 2017 et 2020 dans l’équipe MΞDISIM, jointe entre l’INRIA et le Laboratoire de Mécanique des Solides de l’École polytechnique. Sa thèse, intitulée Mécanique pulmonaire personnalisée : modélisation, estimation et application à la fibrose pulmonaire, a été réalisée sous la direction de Dominique Chapelle et Martin Genet, dans le cadre de l’école doctorale de l’Institut polytechnique de Paris. La thèse s’est déroulée en étroite collaboration avec des médecins, pneumologues et radiologues, de l’hôpital APHP Avicenne de Bobigny.
Au cours de sa thèse, Cécile a aussi participé à plusieurs événements de vulgarisation scientifique, comme la Fête des Sciences, afin de partager avec les jeunes son intérêt pour les sciences.
Pour la récompenser de son parcours et ses travaux de recherche, Cécile a été récompensée par le prix Jeunes Talents France 2020 de la fondation l’Oréal et l’Unesco.
Cécile a soutenu sa thèse le 18 décembre 2020 en visioconférence, devant un jury constitué de Wolfgang A. Wall (président du jury), Stéphane Avril (rapporteur), Aline Bel Brunon, Nicolas Triantafyllidis, Pauline Assemat, Jean-Francois Bernaudin, Martin Genet et Dominique Chapelle.
Pour plus d’information sur la thèse et un accès à la version numérique du manuscrit de thèse, le lien suivant peut être consulté : http://www.theses.fr/2020IPPAX076.
Présentation du laboratoire d’accueil
MΞDISIM est une équipe-projet Inria, jointe avec l’École polytechnique au sein du Laboratoire de Mécanique des Solides (UMR7649 CNRS/INSIS — Institut polytechnique de Paris) et du centre de recherche Inria Saclay-Île-de-France, situé sur le campus de l’École polytechnique. Elle est dirigée par Philippe Moireau.
L’équipe développe des méthodes mathématiques et numériques originales dans le domaine de la modélisation biomécanique des tissus et des organes, avec un focus non exclusif sur le système cardiovasculaire. Les contributions comprennent donc : (1) la modélisation à la fois multiphysique et multiéchelle des systèmes d’intérêt ; (2) des méthodologies de problèmes inverses, afin de tirer parti des différentes données disponibles pour compenser les nombreuses incertitudes inhérentes à de tels systèmes naturels ; (3) des procédures numériques spécifiquement formulées et analysées pour être efficaces pour les types de problèmes directs et inverses considérés ; et (4) des études expérimentales et des applications cliniques, réalisées tant au sein de l’équipe qu’à travers diverses collaborations. Il s’agit donc d’une équipe pluridisciplinaire, au carrefour des mathématiques appliquées, de la mécanique, de la bioingénierie et des applications médicales.
Plus d’information sur le site internet de l’équipe : https://m3disim.saclay.inria.fr/