Nanobiologie : comprendre le vivant et agir sur lui

REPÈRES
Le dernier prix Nobel de chimie attribué à S. Hell, E. Betzig et W. Moerner pour leurs travaux sur la microscopie à superrésolution a révélé l’importance de ces technologies permettant de sonder optiquement les structures biologiques aux échelles comprises entre 10 nm et 1 μm. En effet, les dimensions d’une protéine sont de l’ordre du nanomètre tandis qu’une cellule mesure typiquement une dizaine de microns.
Un des enjeux principaux de la biologie est de comprendre le fonctionnement de cette petite usine qu’est la cellule. Les outils usuels de la biologie permettent d’aborder cette question aux deux extrémités : à l’échelle moléculaire, ou au niveau de la cellule, comme si cette usine cellulaire était décrite par une photographie d’ensemble et un zoom sur sa visserie.
La cellule, une nano-usine
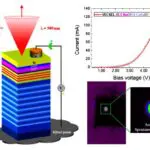
Neurone de rat en culture dont des récepteurs au GABA (un neurotransmetteur) sont marqués par des nanocristaux semi-conducteurs CdSe/ Zns. La taille réelle du neurone est d’une dizaine de microns.
L’échelle naturelle de compréhension de la biologie est ainsi celle des nanosciences (entre 1 nm et 1 μm), où la dynamique de la signalisation cellulaire peut être observée. Ce niveau d’observation et de contrôle est cependant longtemps resté inaccessible.
Ces considérations, et le développement de nanomatériaux et de méthodes d’observation nanoscopiques, permettent l’émergence de la nanobiologie. Elle désigne l’utilisation de techniques ou d’objets issus des nanosciences pour la biologie – la bionanotechnologie – mais aussi l’étude nouvelle de la dynamique des phénomènes biologiques aux échelles nanométriques – la biologie nanométrique.
Bionanotechnologie
La biologie en laboratoire et le diagnostic médical s’appuient sur des méthodes analytiques permettant de révéler la présence de biomolécules dans des échantillons par la reconnaissance spécifique de la cible par un agent de marquage souvent couplé à des molécules organiques luminescentes.
Cependant, ces molécules se dénaturent rapidement sous illumination suivant un phénomène appelé photoblanchiment. Cela limite fortement la sensibilité de détection et le suivi dans le temps d’un processus biologique.
Détection in vivo et in vitro
Dans ce contexte, l’utilisation de nanoparticules, comme des nanocristaux semi-conducteurs, des nanoparticules de terres rares, ou des nanodiamants, a été développée depuis le début des années 2000.
“ L’échelle naturelle de compréhension de la biologie est celle des nanosciences ”
Leurs propriétés optiques exceptionnelles, en termes de photostabilité et de luminosité, ont permis la détection de biomolécules in vitro et in vivo, avec des performances sensiblement supérieures aux systèmes existants. Ces outils se popularisent ainsi dans les laboratoires spécialisés en remplacement des marqueurs organiques traditionnels.
La production de particules à contraste multiple (luminescence, IRM, rayons X, etc.) permet alors de constituer une nouvelle « boîte à outils » pour l’imagerie biologique. Elles seront vraisemblablement bientôt mûres comme technologies de substitution à celles existant pour le diagnostic médical.
Théranostique
Des nanoparticules ont par ailleurs été utilisées pour des applications médicales comme marqueurs ou comme transporteur d’une substance active. Des polymères peuvent ainsi former des particules d’encapsulation et adresser spécifiquement un traitement vers un site spécifique.
L’association de la mesure pour le diagnostic et de la thérapie adaptée par un même dispositif constitue un nouveau champ, la théranostique. Les nanotechnologies peuvent jouer un rôle essentiel dans son développement en permettant de combiner ces multiples fonctions sur une unique plateforme.
Biologie nanométrique
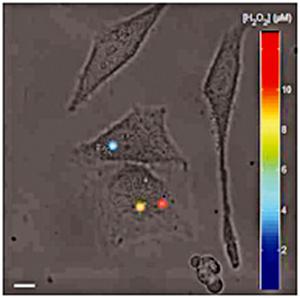
Cellule tumorale humaine (HeLa) placée dans un gradient de facteur de croissance ayant internalisé des nanoparticules YVO4:Eu dont la luminescence mesure la concentration en espèces oxydantes indiquée par le code couleur. La barre d’échelle indique 5 μm.
Au-delà de l’aspect technologique, changer d’échelle pour sonder la machinerie cellulaire au niveau nanométrique peut contribuer à sa compréhension, en renouvelant conceptuellement sa description.
Des nanoparticules ont été utilisées comme marqueurs biologiques pour suivre la dynamique de molécules individuelles à l’intérieur d’une cellule. Le nombre de molécules impliquées dans un processus cellulaire étant souvent faible, cette approche a permis de révéler des modalités de transduction du signal cellulaire encore inconnues, concernant par exemple l’organisation synaptique.
L’observation résolue à la fois dans le temps et l’espace de la signalisation cellulaire, c’est-à-dire le suivi dynamique des interactions moléculaires mises en jeu dans la réponse cellulaire à une modification de son environnement est essentielle et désormais possible par l’utilisation de l’imagerie superrésolue ou de molécules individuelles.
Nanosondes
Des nanoparticules ont également été utilisées comme nanosondes intracellulaires pour réaliser des cartographies dynamiques d’une réponse cellulaire avec une précision de localisation spatiale de l’ordre d’une dizaine de nanomètres.
“ Des nanoparticules ont été utilisées comme marqueurs biologiques »”
L’utilisation de nanoparticules de YVO4:Eu, dont la luminescence est modulée par la présence d’oxydants, a ainsi permis de suivre la production locale d’espèces oxygénées réactives en réponse au signal d’un facteur de croissance.
Des nanotubes de carbones greffés sur des surfaces ont également été utilisés dans le même objectif. Il est ainsi possible de réaliser un dosage dans un volume nanométrique à l’intérieur d’une cellule pour sonder un signal localisé et éventuellement évaluer l’impact d’un traitement thérapeutique à l’échelle moléculaire.
Nanocontrôle
Le contrôle à cette échelle est une étape supplémentaire et le positionnement subcellulaire de nanoparticules magnétiques greffées à des protéines a par exemple permis d’induire une réponse cellulaire localisée.
LE PARI DE GOOGLE
Les applications dans le champ émergent de la médecine personnalisée sont considérables en ouvrant la possibilité d’une mesure ciblée dont les résultats instantanés conditionnent le choix et/ou l’intensité de la thérapie.
Cela constitue un nouveau paradigme, remplaçant le diagnostic par le suivi continu individualisé, qui est déjà exploré notamment par Google.
Les dispositifs micro et nanofluidiques peuvent créer des stimulations structurées dans l’espace tandis que les systèmes électroniques miniaturisés permettent le contrôle et la mesure de l’activité électrique avec une résolution subcellulaire. L’association de ces outils permet alors d’envisager des études portant sur des systèmes cellulaires complexes contrôlés, dans une approche de type organ on chip avec une précision nanométrique pour le suivi de leur activité.
Ces avancées permettent d’envisager la mesure et le contrôle nanométrique des voies de signalisation dans une cellule choisie, qui sera une approche puissante pour le diagnostic et la conception de traitements innovants.
La nanobiologie ouvre ainsi la voie, au-delà de la médecine personnalisée, vers la nanomédecine, où l’action thérapeutique serait localisée à l’échelle subcellulaire.
Les atouts de Paris-Saclay
La nanobiologie se situe à une convergence entre science des matériaux, biologie moléculaire, cellulaire et systémique. La capacité de créer une synergie entre les multiples compétences nécessaires, déjà présentes au plus haut niveau international à Paris-Saclay, à commencer par l’affirmation de la nanobiologie comme discipline au niveau de la recherche et de l’enseignement, semble essentielle pour aborder cette nouvelle frontière.