Alexandre de Chancourtois (X1838), précurseur de Mendeleïev


L’Unesco a proclamé 2019 Année internationale du tableau périodique des éléments chimiques, pour marquer le 150e anniversaire de la publication dans laquelle Dmitri Mendeleïev (1834−1907) présentait son premier tableau périodique. Pour autant, Mendeleïev n’était pas le premier à mettre en évidence une périodicité dans les propriétés des éléments en fonction de leur masse. Ce mérite revient à Alexandre-Émile Béguyer de Chancourtois (X1838), qui a proposé en 1862 un classement des éléments basé sur une hélice tracée sur un cylindre, dite « vis tellurique ».
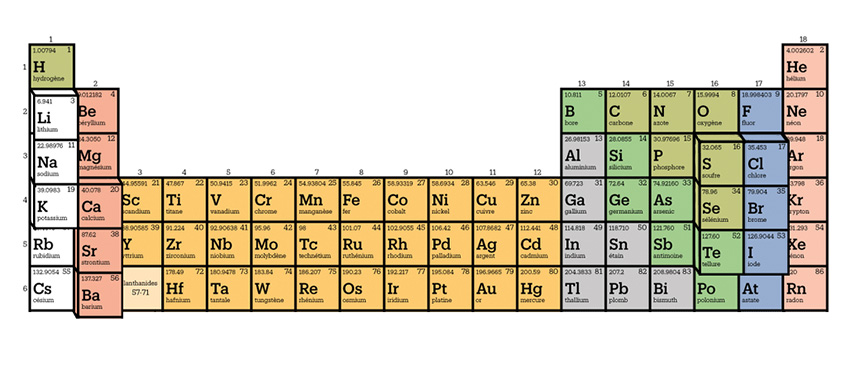
Lavoisier ayant établi la notion moderne d’élément chimique en 1789, les chimistes ont très vite cherché à classer les éléments en fonction de leurs propriétés chimiques. Par exemple, la famille des métaux alcalins (lithium, sodium, potassium…), celle des métaux alcalinoterreux (béryllium, magnésium, calcium, strontium, baryum…) et celle des halogènes (fluor, chlore, brome, iode) préfiguraient en quelque sorte les colonnes 1, 2 et 17 du tableau périodique actuel, qui en comporte 18.
Les premiers balbutiements
En parallèle de ces recherches basées sur les propriétés chimiques, les chimistes menaient des recherches quantitatives, c’est-à-dire basées sur la notion de masse atomique qui s’affinait progressivement.
Les recherches quantitatives ont continué dans les années 1850. On trouvait alors de plus en plus de rapports numériques entre les masses des éléments, non seulement à l’intérieur de familles chimiques, mais aussi entre familles voisines. Pour établir un tableau périodique, il aurait suffi de regrouper ces familles en ordonnant les éléments par masses croissantes. Encore fallait-il y penser ! Cette démarche, il est vrai, se heurtait au fait que les masses atomiques dont disposaient alors les chimistes étaient peu fiables, car les méthodes de détermination n’étaient pas encore satisfaisantes.
Pourtant, dans les années 1860, des progrès très rapides allaient être réalisés dans l’établissement de la classification. Il est possible que cela soit dû aux travaux du congrès international de Karlsruhe de 1860, qui ont permis de mettre de l’ordre dans les déterminations des masses atomiques et ont favorisé un consensus dans ce domaine entre les chercheurs des différents pays. D’autre part, la découverte rapide de nouveaux éléments, notamment grâce à la spectroscopie, a facilité les recherches de classification. C’est dans ce contexte que la démarche innovante de Chancourtois a abouti à la première véritable mise en évidence d’une périodicité.
REPÈRES
Lorsque Mendeleïev publie son célèbre tableau en 1869, on ne connaît encore que 62 éléments. Son génie a été de prévoir l’existence d’éléments encore inconnus, effectivement découverts par la suite, et situés désormais aux emplacements qu’il avait prévus dans son tableau. Cependant, Alexandre-Émile Béguyer de Chancourtois (1820−1886) avait proposé dès 1862 un classement des éléments basé sur une hélice tracée sur un cylindre, dite « vis tellurique ». Ce premier système périodique n’était pas aussi performant que celui publié par Mendeleïev en 1869, mais il n’en constituait pas moins une innovation majeure.
Un géologue égaré parmi les chimistes
Professeur de géologie à l’École des mines
Chancourtois, X1838 et ingénieur des Mines, fut professeur de géologie à l’École des mines de Paris, et président de la Commission de la Carte géologique détaillée de France. Après des expéditions géologiques en Europe de l’Est et en Asie centrale, il a enseigné à partir de 1852 la géologie, d’abord en tant qu’adjoint d’Élie de Beaumont, puis comme titulaire de la chaire en 1875 [cf. sa nécrologie, Annales des Mines 1887, 11, p. 505.3]. En travaillant sur ce cours, il cherchait un moyen de présenter de manière logique toutes les notions relatives aux roches et à leurs constituants.
C’est finalement lui qui a eu l’idée d’ordonner les éléments par masses croissantes : il les a alignés le long de segments inclinés à 45° pour constituer un tableau que l’on peut qualifier d’oblique. Ainsi, il a correctement placé les colonnes 1, 2, 13, 14, 15, 16 et 17 : le chlore se trouvait positionné directement en dessous du fluor, le calcium en dessous du magnésium et le silicium en dessous du carbone, par exemple. Ensuite, il a formé un cylindre en enroulant ce tableau de sorte que les segments constituent une ligne hélicoïdale continue ; les familles se trouvaient alors sur les génératrices du cylindre. Toutefois, le tableau devenait faux à partir du calcium, car la méthode ne convenait pas pour le classement des métaux de transition (les futures colonnes 3 à 12).
Malgré ces insuffisances, ce fut la première classification montrant que, lorsque les éléments sont ordonnés selon leur masse croissante, les propriétés chimiques reviennent périodiquement. Il s’agit donc du premier véritable système périodique.
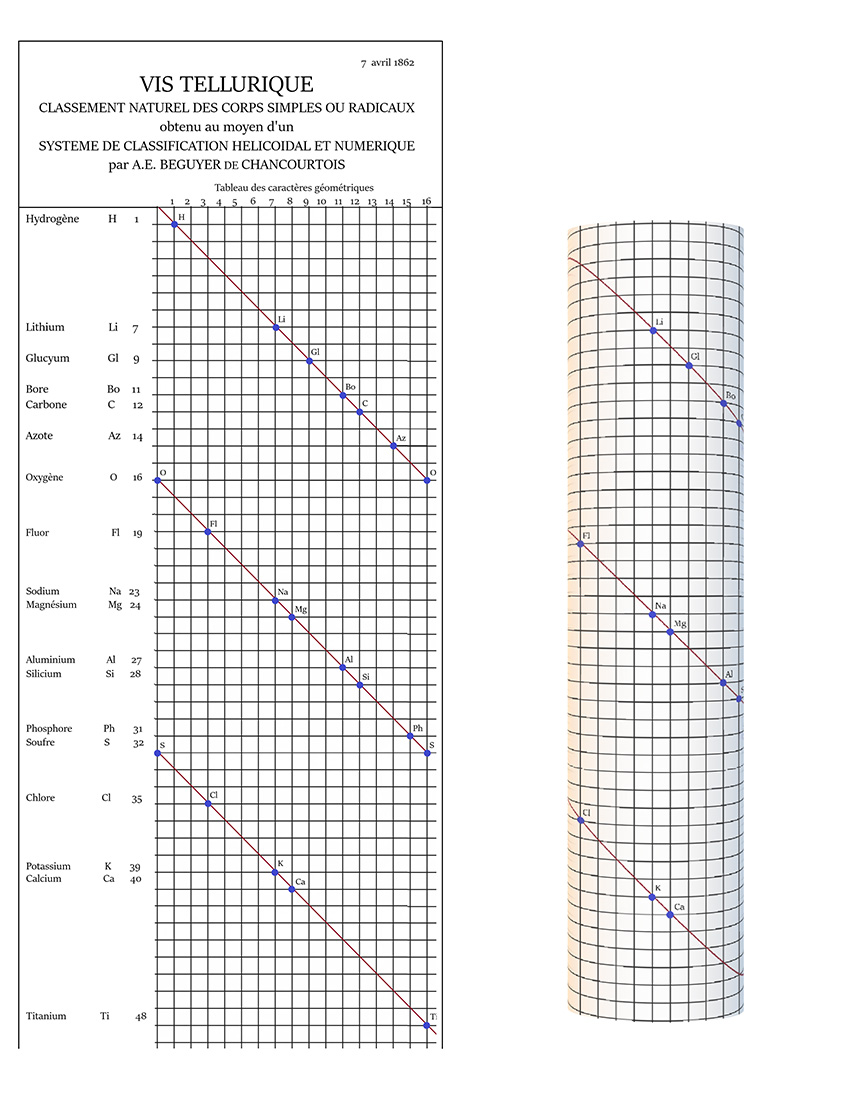
La vis tellurique
Chancourtois a nommé sa classification vis tellurique : « D’après son mode de réalisation et son origine, je lui donne le nom significatif de vis tellurique », écrit-il dans le rapport à l’Académie des sciences du 7 avril 1862. Un peu plus tard, le 5 mai de la même année, tout en précisant que le nom lui a été suggéré surtout par la place centrale de l’élément tellure sur la vis, il écrit que « l’épithète tellurique (…) rappelle très heureusement l’origine géognostique, puisque tellus signifie terre dans le sens le plus positif, le plus familier, dans le sens de terre nourricière ». Ce propos montre bien que la géologie était le point de départ des réflexions de Chancourtois. Il voyait la forme hélicoïdale comme étant idéale pour représenter une périodicité : ainsi, il a utilisé des méthodes comparables pour rechercher une logique mathématique dans les relations entre les différentes formations géologiques de la Terre.
Priorité aux nombres
Chancourtois avait aussi une vision mathématique de la matière, selon laquelle « les propriétés des corps sont les propriétés des nombres » (cf. son ouvrage de 1863, La Vis tellurique). Cette vision pourrait expliquer la priorité qu’il donnait aux nombres plutôt qu’aux appartenances à une famille chimique. Ainsi Chancourtois n’a pas correctement placé l’iode en dessous du chlore et du fluor comme l’ont fait ses successeurs : le piège, c’est que, curieusement, l’iode (aujourd’hui élément 53) est plus léger que le tellure (aujourd’hui élément 52). De plus, cette vision mathématique le conduisait à tenter de prédire des propriétés chimiques à partir d’une factorisation des masses des éléments, supposées entières. Dans cet esprit, il aurait aimé rapprocher la notion d’élément de celle de nombre premier.
Une classification imparfaite
L’approche étonnante de Chancourtois et les nombreuses imperfections dans sa classification pourraient expliquer en partie le fait que la vis tellurique n’ait pas eu autant de reconnaissance que le tableau de Mendeleïev. Pourtant, cette première classification périodique a ses mérites. L’importance du numéro atomique aujourd’hui confirme en quelque sorte l’intuition de Chancourtois qui voyait un rapport étroit entre les nombres et la nature des corps. De même, son idée que ces nombres pouvaient servir à prédire et à expliquer les spectres de raies des éléments avait un côté prophétique : c’est au fond ce qu’apportera en 1913 la loi de Moseley reliant les fréquences (ν) des raies au numéro atomique (Z) de l’élément. Toutefois, l’intérêt de cette vis tellurique n’a pas été véritablement perçu à l’époque, d’autant plus que Chancourtois ne faisait pas partie du cercle des chimistes.
Les triades entrent en scène
En 1817, le chimiste allemand Döbereiner identifie une première « triade » : trois éléments alcalinoterreux (calcium, strontium et baryum) dont la masse de l’élément du milieu est égale à la moyenne des masses des deux autres. Ce concept prend corps avec trois autres triades publiées en 1829, alignant des éléments qui sont superposés dans le tableau périodique actuel. C’est la première découverte de rapports quantitatifs entre les masses d’éléments d’une même famille, et donc en quelque sorte un premier pas vers le tableau périodique actuel, où ces rapports se comprennent directement. En 1843, Gmelin combine pour la première fois des triades (c’est d’ailleurs lui qui a trouvé ce nom) dans un tableau comportant 55 éléments. Bien qu’on ne puisse pas encore considérer cette classification comme étant périodique, elle regroupait déjà correctement les éléments des futures colonnes 1, 2, 15, 16 et 17 du tableau actuel, du moins pour ses trois premières lignes.
De Chancourtois à Mendeleïev
Pendant les sept années suivant la publication de la vis tellurique par Chancourtois, quatre chimistes ont développé des tableaux périodiques de plus en plus corrects. Pour la plupart, ces classifications devenaient erratiques, comme celle de Chancourtois, à partir de la 3e ligne : alors que les éléments des colonnes 1, 2 et 17 appartiennent, comme on l’a vu au début de cet article, à des familles chimiques relativement faciles à identifier, il était beaucoup plus difficile de classer correctement les métaux de transition. En 1865, Odling était le premier à séparer ces métaux de transition des autres colonnes. Pourtant, il fallut encore quelques années avant d’arriver à des tableaux prenant en compte ces éléments : celui de Lothar Meyer (1870), où préfiguraient neuf colonnes, et celui de Mendeleïev (1869), comportant les dix colonnes de métaux de transition.
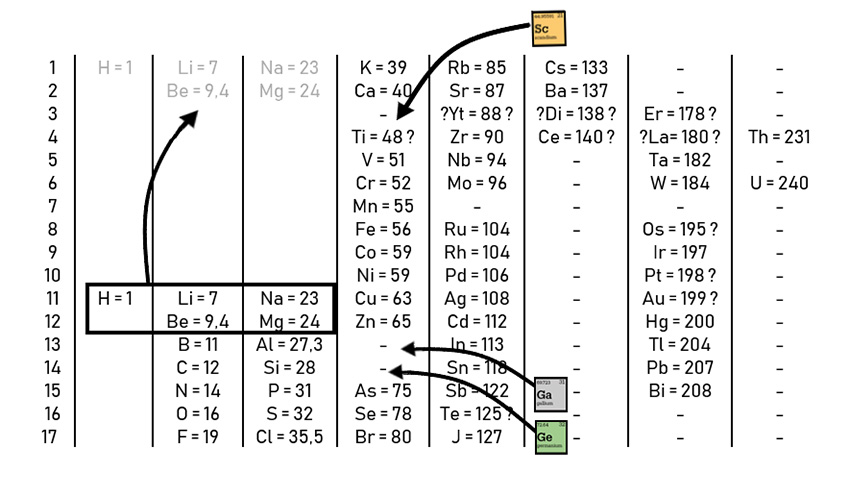
Le tableau de Mendeleïev était le premier à être composé de 17 colonnes – de 17 lignes en fait, puisque sa présentation était horizontale. Pour cette classification, Mendeleïev a ordonné les éléments par masses croissantes, sauf lorsque, exceptionnellement, cela contredit les ressemblances chimiques : ainsi, il a inversé les places de l’iode et du tellure pour respecter leur appartenance à des familles chimiques (ce que Chancourtois n’avait pas fait). Il a aussi ajusté les masses du béryllium et de l’uranium en fonction de leurs places dans le tableau. Mendeleïev a donc pu utiliser sa classification pour identifier des erreurs dans les mesures de masses des éléments !


Des prédictions fructueuses
Mendeleïev n’a pas seulement classifié des éléments déjà connus. De manière extrêmement précise, il a prédit très vite certaines propriétés de trois éléments encore inconnus qu’il nommait l’eka-aluminium, l’eka-bore et l’eka-silicium (cf. E. Scerri, The Periodic Table, Oxford, 2007). Trois découvertes ont confirmé ces prédictions : l’eka-aluminium a été découvert sous le nom de gallium en 1875 par Lecoq de Boisbaudran, l’eka-bore sous le nom de scandium par Nilson en 1879 et l’eka-silicium sous le nom de germanium par Winkler en 1886. Le fait que ces éléments aient été effectivement trouvés a considérablement contribué à la célébrité de Mendeleïev et de son tableau. Ces trois éléments sont les trois principales prédictions de Mendeleïev.
Plus tard, il fera d’autres prédictions, dont cinq correctes (polonium, technétium, rhénium, francium et protactinium) mais moins précises que les premières, et… huit fausses (notamment 2 éléments qui seraient plus légers que l’hydrogène). Toutefois, il était pratiquement impossible pour Mendeleïev de prévoir la 18e colonne du tableau actuel. Ce sont le chimiste Ramsay et le physicien Rayleigh qui ont montré en 1900 que les gaz nobles constituaient cette 18e colonne qui venait compléter le tableau, un peu comme la clé de voûte qui manquait encore pour assurer la stabilité d’un édifice.
“Gallium, scandium et germanium sont les trois principales prédictions
de Mendeleïev”
Épilogue numérique
On peut s’étonner d’un tel contraste entre la célébrité de Mendeleïev et l’oubli dans lequel est tombé Chancourtois. Celui-ci est pourtant indéniablement l’initiateur du concept de périodicité. Il faut admettre que Mendeleïev, en clarifiant le tableau jusqu’à
17 colonnes et en étant capable de prédire des éléments futurs, a donné sa véritable dimension au tableau tel qu’il est connu aujourd’hui (à part la 18e colonne). Cependant, en célébrant les 150 ans de la publication majeure de Mendeleïev, il est bon de rappeler que 2019 est aussi le 157e anniversaire de la Vis tellurique de Chancourtois.
Références
Scerri, E., The Periodic Table : Its Story and Its Significance, Oxford University Press, 2007.
Van Spronsen, J. W. L’histoire de la découverte du système périodique des éléments chimiques et l’apport de Béguyer de Chancourtois, Conférence donnée au Palais de la découverte, Alençon : Bernard Grisard, 1965.
Fuchs, E., « Notice nécrologique sur M. A.-E. Béguyer de Chancourtois, inspecteur général des mines », Annales des Mines 1887, 11, p.505.
Chancourtois, A.-E. Béguyer de, Vis tellurique, classement naturel des corps simples ou radicaux obtenu au moyen d’un système de classification hélicoïdal et numérique, Paris : Mallet-Bachelier, 1863.
Mendeleïev, D. I., « Die periodische Gesetzmässigkeit der chemischen Elemente », Annalen der Chemie und Pharmacie, 1872, vol. suppl. 8(2), p. 149.
Brock, W. H, The Fontana History of Chemistry, London : Fontana Press, 1992, p. 323–325.






