Voyage aux frontières de la physique avec la biologie

A la croisée de la physique et de la biologie se trouve la biophysique cellulaire qui considère la cellule certes programmée par ses gènes, mais aussi comme un matériau mou, déformable, et actif que l’on peut étudier par simulation. On peut ainsi analyser les cellules sous contraintes, comme dans une tumeur ou mimer le mouvement d’une bactérie dans une cellule.
Les mouvements et les déformations cellulaires ont toujours fasciné biologistes et physiciens, et ces deux communautés ont toujours été de front pour comprendre les observations du « vivant ».
En particulier, Robert Brown en 1827 observe que des particules de pollen en solution dans l’eau sont animées d’un mouvement incessant. Le contexte historique de cette découverte aide à comprendre dans quelles dispositions intellectuelles étaient Brown et ses collègues et comment leur raisonnement s’est d’abord engagé dans la voie d’une « force vivante » de ces particules de pollen animées, qui se sont révélées ensuite être parfaitement inertes.
REPÈRES
Nouveau champ de recherche, la biophysique cellulaire considère la cellule pas seulement comme un objet simplement programmé par ses gènes, mais aussi comme un matériau mou, déformable, et actif.
Contrairement aux matériaux habituels, qui sont à l’équilibre et donc inertes, nos cellules contiennent en effet une source d’énergie : l’hydrolyse de l’ATP (adénosine triphosphate). Cette propriété en fait des matériaux hors d’équilibre, capables d’une activité propre.
PAS DE « FORCE VIVANTE » DANS LE MOUVEMENT BROWNIEN
Le début du XIXe siècle voit en effet naître la « théorie cellulaire » selon laquelle tout être vivant est formé de cellules vivantes. Le même Robert Brown observe des tissus vivants à l’aide des microscopes optiques de plus en plus performants, et il est d’ailleurs le premier à décrire dans des cellules animales la présence d’une masse sombre et arrondie, le noyau (d’abord appelé nucléoplasme), en 1831.
LA « MATIÈRE MOLLE »
La Matière molle a été ainsi nommée par le pionnier de ce domaine, Pierre-Gilles de Gennes, prix Nobel de physique 1991. C’est à partir de ses travaux que l’Institut Curie s’est inspiré de la physique des objets mous (polymères, liquides, mécanique des fluides, matériaux visqueux, élastiques, ou viscoélastiques, etc.) pour éclairer, par de nouvelles approches, les mécanismes des fonctions cellulaires comme leur division et leur mouvement.
Ce n’est finalement qu’à la fin des années 1880 que des expériences plus systématiques montrent que le mouvement est plus rapide lorsque la taille des particules est plus petite, et que le mouvement est ralenti dans un solvant plus visqueux.
Ensuite, au début du XXe siècle, avec Einstein en 1905 et Jean Perrin en 1908, on comprend que ces particules apparaissent plus agitées lorsqu’on augmente la température : l’énergie thermique (quelques kBT, i.e. quelque 4 10-21 joules) est transférée à ces petits objets en solution sous forme d’énergie cinétique, et c’est pourquoi ils sont en mouvement, appelé « mouvement brownien ».
De nouvelles observations sur les cellules animent actuellement les communautés de biologistes et de physiciens, en particulier avec les progrès extraordinaires, ces dernières décennies, des techniques de microscopie et de la connaissance de la génétique, et donc des molécules qui composent le vivant.
Les vingt dernières années ont vu les physiciens envahir les laboratoires de biologie pour s’attaquer à comprendre la motilité cellulaire (motilité : mouvement d’un organisme vivant), la déformabilité des cellules, et leur capacité à répondre à des sollicitations mécaniques.
S’INSPIRER DE LA « MATIÈRE MOLLE »
Ces nouveaux venus ont une approche différente de leurs récents prédécesseurs, qui ont introduit dans les sciences du vivant les rayons X, les lasers, les IRM, les ultrasons, maintenant couramment utilisés dans les hôpitaux et les laboratoires. Cette nouvelle vague de physiciens est issue de la « matière molle ».
Ce ne sont pas tant des nouveaux outils que ces physiciens apportent dans les laboratoires de biologie cellulaire, mais une nouvelle manière de penser, différente de l’approche purement génétique, prenant plutôt en compte les propriétés d’autoassemblage des protéines, les propriétés mécaniques de ces assemblages, leur capacité à se réorganiser, se déformer, s’adapter.
Deux approches se sont développées, dans ce cadre : l’une consiste à manipuler directement les cellules par des méthodes mécaniques et en analyser les conséquences sur leur comportement ; l’autre à reconstituer les fonctions cellulaires à partir d’éléments purifiés.
DU COMPLEXE AU SIMPLE, ET VICE-VERSA
Dans la première approche, on suit les réponses mécaniques des cellules soumises à des contraintes externes contrôlées. Il s’agit alors de marquer, surexprimer, inhiber ou même éliminer des éléments connus et observer comment la cellule change de forme, modifie son mouvement. La cellule est alors « simplifiée » peu à peu, et l’effet de ces altérations est caractérisé.
LES MICROFILAMENTS D’ACTINE
L’actine est une protéine biglobulaire de 5,46 nm de diamètre présentant un rôle important pour l’architecture et les mouvements cellulaires. Les filaments d’actine s’assemblent à partir de leur forme monomérique, également appelée G‑actine pour l’actine globulaire. Ils sont hélicoïdaux (comme de nombreuses structures biologiques) et ont une épaisseur de 4 à 7 nanomètres. Leur longueur peut aller jusqu’à la taille cellulaire, de l’ordre de 10 micromètres. Ils sont responsables de la plupart des processus de la motilité cellulaire.
Cette approche, nommée top-down, présente l’avantage d’utiliser la cellule entière et de rester proche de la réalité complexe. Le seul désavantage est qu’il est difficile d’extraire la contribution exacte de chaque composant, en interaction avec la multitude.
La deuxième approche est inversée et, par conséquent, appelée approche ascendante ou bottom-up. Elle s’inspire de la célèbre citation du physicien Richard Feynman : What I cannot create I do not understand, et consiste à recréer le comportement des cellules par l’addition successive de composants purifiés et identifiés.
La construction d’un système reconstitué, également appelé système biomimétique, est conçue pour reproduire chaque module de la cellule individuellement.
Cette approche biomimétique conduit à un système expérimental parfaitement contrôlé et permet des mesures quantitatives dans des conditions bien maîtrisées, à partir desquelles des modèles théoriques peuvent être développés et des prévisions physiques ou mécaniques peuvent être validées.
À LA BASE DE LA DÉFORMABILITÉ DE NOS CELLULES : LE CYTOSQUELETTE
Nos cellules sont constituées, simplement, d’une membrane (bicouche de lipides tête-bêche) qui renferme le cytoplasme. Elles ont la capacité de maintenir leur structure et leur intégrité, mais peuvent également changer de forme tout au long de leur vie.
LA MOTILITÉ CELLULAIRE
La motilité cellulaire peut être décomposée dans un mécanisme à trois étapes : d’abord, la membrane au niveau du front de la cellule active la polymérisation de l’actine, elle est donc poussée par l’assemblage de l’actine en filaments ; puis la cellule adhère au substrat environnant ; enfin l’arrière de la cellule est contracté par l’action de moteurs moléculaires sur le réseau d’actine, qui se traduit par une accumulation de tension.
Ces changements de forme se produisent au cours de fonctions cellulaires telles que la circulation, la motilité ou la cytocinèse qui correspond à l’étape ultime de la division cellulaire.
Les déformations cellulaires sont dues à l’activité de biopolymères ou filaments cytoplasmiques constituant ce qui est appelé le « cytosquelette », étroitement couplé aux membranes cellulaires. Le cytosquelette s’autoassemble et se désassemble en permanence à l’intérieur des cellules en utilisant l’énergie biochimique de la cellule : l’adénosine triphosphate (ATP) qui est hydrolysée en adénosine diphosphate (ADP).
Ce cytosquelette est donc une architecture cellulaire dynamique, en constante réorganisation, permettant des changements de forme des cellules pendant leur durée de vie ou en réaction à des signaux environnementaux. Le cytosquelette est composé de trois familles.
Celle qui nous intéressera dans cet article est constituée de filaments d’actine ou microfilaments. Une autre famille du cytosquelette est celle des microtubules qui sont des filaments creux, composés de 13 protofilaments, largement utilisés comme pistes dans le trafic de cellules. La dernière famille est celle des filaments intermédiaires, moins bien connus, mais qui ont un rôle dans la mécanique des cellules et en particulier la mécanique de l’enveloppe nucléaire.
FIGURE 1
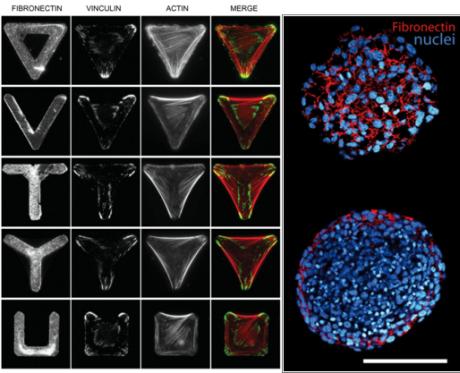
À gauche : le cytosquelette réagit à l’asymétrie des micropatrons adhésifs (fibronectine : « colle » cellulaire). Le marquage par fluorescence de l’actine et de la vinculine (protéine cellulaire reliant le cytosquelette d’actine aux zones d’adhésion) révèle une organisation isotrope des fibres d’actine sur un cadre triangulaire (rangée supérieure).
En revanche, la répartition spatiale des fibres de contrainte est anisotrope sur les micropatrons en [V], [T], [trépied] ou [U] (de haut en bas). Les adhésions (marquage vinculine) sont concentrées sur des sommets des patrons où les fibres d’actine s’accumulent. La longueur du bord du triangle est de 46 micromètres. D’après Théry et al, Cell Motility and the Cytoskeleton (2006).
À droite : images confocales (observations dans un plan donné) de sphéroïdes libres (en haut) et confinés (en bas) après cryosection et immunomarquage pour DAPI (bleu, marque les noyaux des cellules), et fibronectine (rouge). Barre d’échelle : 100 micromètres. D’après Alessandri et al, PNAS (2013).
SE PROPULSER EN PROJETANT DES FILAMENTS D’ACTINE
La membrane est le site de nombreuses réactions biochimiques, en particulier pour l’activation de la polymérisation des filaments d’actine. Le mouvement cellulaire repose principalement sur la dynamique de ces filaments.
À l’avant de la cellule, des réseaux de filaments d’actine ramifiés et reliés entre eux sont le principal moteur du mouvement cellulaire puisqu’ils poussent la membrane cellulaire par polymérisation contre elle. Une mince couche de filaments d’actine, appelée le cortex cellulaire, recouvre la membrane plasmique à l’arrière et sur les côtés de la cellule, ce qui est important pour le maintien et les changements de forme cellulaire.
Le reste de la cellule contient un réseau tridimensionnel de filaments entrecoupés de faisceaux contractiles, qui relient le cytosquelette cellulaire à la matrice extracellulaire via des sites d’adhérence.
La contraction dans la cellule est produite par des moteurs moléculaires qui provoquent un glissement des filaments d’actine les uns par rapport aux autres, et donc une contraction globale du cortex cellulaire, mettant ainsi les cellules sous tension.
La migration cellulaire s’adapte à son environnement par la coordination des trois étapes de la motilité, et tandis que la motilité cellulaire permettant aux cellules de « ramper » sur la matrice extracellulaire repose essentiellement sur les deux premières étapes, la motilité cellulaire permettant aux cellules de passer au travers de petits interstices repose principalement sur la troisième étape, où la contractilité a un rôle crucial.
DES « MICROPATRONS » POUR MESURER LA MOTILITÉ

Les « perles de saveurs » sont utilisées dans les plats raffinés des plus grands cuisiniers. © M.STUDIO / FOTOLIA.COM
BIOPHYSIQUE ET GASTRONOMIE
Les boules d’alginate sont très largement utilisées en ingénierie alimentaire, pour ce qui s’appelle les « perles de saveurs », que vous trouvez dans les plats raffinés des plus grands cuisiniers. Ces perles de saveurs sont de petites sphères gélifiées (pellicule d’alginate : dérivé de l’algue Kombu) contenant un cœur liquide qui se décline en multiples saveurs. Elles éclatent en bouche et libèrent ces saveurs.
Comment se comportent les cellules une fois soumises à des contraintes mécaniques externes ? Quels sont les assemblages internes du cytosquelette qui permettent aux cellules de s’adapter à ces contraintes mécaniques ? Sachant que les cellules cancéreuses, au sein des tumeurs, sont justement sous contrainte mécanique, comment pourrait-on étudier leur comportement hors d’une tumeur, mais dans des conditions contrôlées qui reproduisent celles des tumeurs ?
Les chercheurs ont mis au point, pour répondre à ces questions, des techniques de « micropatrons » (figure 1, gauche), consistant à mettre les cellules au contact de différentes formes prédéfinies, comme des triangles, des formes en V, T, Y et U. De la fibronectine, une protéine d’adhésion, une sorte de colle pour cellule, permet aux cellules d’adhérer spécifiquement sur ces patrons, alors que le reste de la surface est traité par un antiadhésif.
Un marquage des protéines du cytosquelette montre bien, sur la figure 1 (gauche), que des faisceaux d’actine se forment et ont une structure différente suivant les différents patrons.
La vinculine, qui permet de faire le lien entre les filaments d’actine et la colle extracellulaire (la fibronectine), se trouve aux extrémités des faisceaux de filaments d’actine, permettant ainsi aux cellules d’épouser la forme du patron.
La forme des faisceaux d’actine, leur densité, mesurées par l’intensité de leur fluorescence, la taille des zones d’adhésion, permettent d’en déduire la force exercée par la cellule, qui est observée comme étant proportionnelle à la quantité de protéines présentes dans les zones d’adhésion. Ces expériences permettent donc de quantifier les forces exercées par le cytosquelette en relation avec l’adhésion.
OÙ L’ON JOUE AUX BOULES CELLULAIRES
Une autre approche, cette fois-ci pour mimer des cellules tumorales en croissance, est de confiner un groupe de cellules dans des boules d’alginate.
Ces boules sont biocompatibles, et peuvent être utilisées pour confiner des cellules et les mettre sous contrainte comme elles le sont dans une tumeur (figure 1, droite).
Ainsi, cette figure illustre comment un agrégat de cellules « libres » se comporte différemment d’un agrégat de cellules confinées dans une pellicule d’alginate. On observe en particulier que les cellules se divisent plus rapidement (leur nombre croît plus vite) quand elles sont contraintes que quand elles sont libres.
Également, on observe que la protéine d’adhésion, la fibronectine, est sécrétée par les cellules libres au sein de l’agrégat, mais pas par les cellules confinées. Ce genre d’approche permet de déterminer, dans des conditions expérimentales contrôlées, les différences de comportement des cellules contraintes comme dans une tumeur.
RETOUR VERS LA PHYSIQUE DES POLYMÈRES
La dynamique des filaments d’actine et la mécanique des réseaux d’actine ont, en retour, ouvert des voies pour la physique des polymères, car les filaments d’actine présentent un avantage sur les polymères chimiques : ils font quelques micromètres de long et peuvent être visualisés simplement en microscopie optique, ce qui n’est pas le cas des polymères chimiques, pour lesquels il faut utiliser de grands instruments (rayons X, neutrons).
À leur surface, les bactéries Listeria monocytogenes sont capables de nucléer la croissance de filaments d’actine. © SAGITTARIA / FOTOLIA.COM
Les propriétés mécaniques des réseaux d’actine se sont révélées très frappantes, car elles dépendent de l’échelle de temps à laquelle les échantillons sont observés.
En effet, alors que les réseaux d’actine sont élastiques à temps court (moins de quelques secondes), ils ont la propriété de s’écouler comme un liquide sur un plus long temps. Ce comportement est appelé viscoélastique » et se retrouve aussi dans les cellules.
Au-delà de leurs propriétés mécaniques étonnantes, les réseaux d’actine ont la capacité de se former à la surface interne de la membrane cellulaire, en polymérisant à partir de sites de nucléation. C’est ainsi que ces filaments « poussent » la membrane cellulaire vers l’avant pour le déplacement de la cellule, ainsi que nous l’avons évoqué plus haut.
Ce type de mouvement ou « motilité » par polymérisation de l’actine est détourné par des bactéries pathogènes qui envahissent nos cellules : les bactéries Listeria monocytogenes. À leur surface, ces bactéries sont capables de nucléer la croissance de filaments d’actine, de la même manière que cela se produit à la membrane cellulaire.
Ces bactéries détournent donc la machinerie cellulaire pour leur propre profit, celui de se déplacer dans nos cellules et envahir les cellules avoisinantes par leur mouvement pénétrant.
Elles constituent un système expérimental de choix pour étudier le mécanisme de « mouvement par polymérisation d’actine », qui a fasciné les biophysiciens. Un tel mouvement n’avait jamais été ni conçu ni observé avec des polymères chimiques ou des macromolécules.
Dès qu’elle entre dans une cellule, la bactérie stimule donc la polymérisation de l’actine à sa surface. Les filaments forment alors une sorte de comète bien visible (une dizaine de micromètres de long) à l’arrière de la bactérie qui devient capable – grâce à la force générée par la croissance des filaments d’actine – de se déplacer (60 micromètres par minute est le record absolu), de déformer la membrane plasmique et de passer dans une autre cellule.
 FIGURE 2
FIGURE 2
Microbilles de latex (rayon 2,2 micromètres) propulsées par polymérisation de l’actine dans un milieu de protéines purifiées. Le mouvement des bactéries Listeria est ainsi mimé, avec l’apparition d’une « comète » formée d’un réseau dense de filaments d’actine. Barres d’échelle, 5 micromètres. D’après Paluch et al, Biophysical Journal (2006).
En haut à gauche : une expérience « à deux couleurs », en microscopie optique de fluorescence, consiste à commencer avec de l’actine rouge, puis à ajouter au bout de quelques minutes de l’actine verte. On visualise ainsi que la ligne qui délimite les deux couleurs, initialement sphérique autour de la bille (pointillés), devient ouverte, sous l’effet des propriétés élastiques du réseau d’actine, forcé à se déformer sous l’effet des contraintes internes dues à la croissance du réseau.
En haut à droite, le même échantillon observé en contraste de phase montre que l’expérience à deux couleurs ne modifie pas la densité du réseau d’actine.
En bas : deux lignes sont éteintes (photoblanchies) au cours du mouvement des microbilles (temps indiqué en minutes-secondes), afin de visualiser les déformations dans le réseau en croissance à la surface des billes. La ligne blanchie perpendiculairement à l’axe de la comète est déformée quand elle est éloignée d’une distance inférieure à un diamètre de bille, la ligne plus éloignée n’est pas déformée.
LES CHERCHEURS « MIMENT » LE MOUVEMENT DES BACTÉRIES
Nous nous sommes dit que, puisque aucune protéine de la bactérie – hormis le nucléateur de polymérisation de l’actine – n’était nécessaire, nous pouvions utiliser des systèmes biomimétiques capables de « mimer », dans des conditions in vitro, le mouvement de la bactérie dans une cellule. Nous avons donc remplacé les bactéries par des microbilles de latex.
Une avancée considérable pour des physiciens, désormais aptes à faire varier un grand nombre de paramètres tant pour la bille (taille du rayon, dureté) que pour le matériel biologique (nucléateur, milieu cellulaire).
En plaçant les billes dans un extrait cytoplasmique, on peut en effet observer un nuage de filaments d’actine pousser et s’accumuler autour de la bille d’une façon symétrique puis visualiser la bille faire une percée dans le nuage et être propulsée comme les bactéries (figure 2).
Plusieurs approches montrent aujourd’hui que ce sont les propriétés élastiques du biopolymère – des filaments d’actine organisés en véritables réseaux, ainsi que des filets de pêche à 3 dimensions, ou des réseaux de polymères – qui exercent une pression sur la bille. L’élasticité du réseau en train de se fabriquer à la surface de la bille pousse l’objet vers l’avant.
Nous n’en sommes pas restés là : nous avons joué sur la dureté de la bille. Que se passe-t-il en effet si la bille devient molle et déformable ? Pour cela, nous avons répété la même expérience, mais en utilisant tout simplement de l’huile de cuisine sur laquelle nous avons réussi à greffer le fameux nucléateur de la polymérisation de l’actine.

Les filaments d’actine font quelques micromètres de long et peuvent être visualisés simplement en microscopie optique. © LAVIEJASIRENA / FOTOLIA.COM
Nous observons alors que la bille se déforme sous l’effet de cette pression du réseau d’actine. C’est grâce à ce type d’expérience que l’on peut réussir à obtenir des données quantitatives (force, module élastique, densité, etc.), but de tout physicien travaillant sur les problématiques biologiques.






Commentaire
Ajouter un commentaire
Mécanique des tissus
Et si l’échelle pertinente c’était le tissu ?
En cancérologie les exemples où les échelles micro méso et macroscopiques sont reliées entre elles sont des exceptions (l’équivalent d’une équation à une inconnue et à une dimension). On peut citer la Leucémie Myéloïde Chronique où on peut aller de l’anomalie chromosomique à la thérapie ciblée. Il est une question très gênante aujourd’hui : combien les thérapies ciblées ont elles guéri de patients ? Et pour enfoncer le clou, celui qui fait mal, à quel coût ? Il faut admettre que en cancérologie les lois de la physique (la mécanique en l’occurence) n’ont pas de frontière commune avec les lois de la biologie. C’est pourquoi l’étude des modèles cancérologiques doit s’appuyer sur le seul modèle représentatif de la maladie : le cancer constitué de deux tissus, soit la matrice extracellulaire et le tissu cancéreux lui-même. A l’échelle mésoscopique donc et en y restant.